Conseil d’examen du prix des médicaments brevetés
L’honorable Ginette Petitpas Taylor
Ministre de la Santé
ISSN 2561-0740
Table des matières
Message du président
Aperçu de nos résultats
Raison d’être, mandat et rôle : qui nous sommes et ce que nous faisons
Contexte opérationnel et principaux risques
Résultats : ce que nous avons accompli
Analyse des tendances en matière de dépenses et de ressources
humaines
Renseignements supplémentaires
Annexe : définitions
Notes de fin de document
Message du président
À titre de président intérimaire, j’ai le plaisir de présenter le Rapport sur les résultats ministériels 2016-2017 du Conseil d’examen du prix des médicaments brevetés (CEPMB).
Le CEPMB est un organisme administratif quasi judiciaire indépendant dont le mandat vise à protéger les consommateurs des médicaments brevetés de prix jugés excessifs et à faire rapport aux Canadiens des tendances relatives aux prix de tous les médicaments ainsi qu’aux dépenses des titulaires de brevets dans la recherche et le développement au Canada.
En décembre 2015, le CEPMB a publié son très attendu Plan stratégique 2015-2018, un tournant important dans l’histoire de l’organisation, car il vise à réformer la façon dont le CEPMB s’acquitte de son mandat de protection du consommateur à la lumière des changements importants récents dans son environnement opérationnel. L’année 2016 a marqué le lancement de l’initiative de consultation Repenser les Lignes directrices, qui constitue une première étape clé des mesures du CEPMB pour moderniser son cadre réglementaire. Les consultations dirigées par le CEPMB se poursuivront après la publication prévue, à l’automne 2017, des modifications proposées par la ministre de la Santé au Règlement sur les médicaments brevetés dans la Partie I de la Gazette du Canada.
Le CEPMB a mené un grand nombre d’activités de conformité et d’application de la loi en 2016 en raison de sa décision de remettre l’accent sur la réglementation axée sur les consommateurs, ce qui a mené à l’acceptation de huit engagements de conformité volontaire et au remboursement de recettes excessives totalisant 35 856 156,83 $ en plus de la réduction des prix des médicaments visés.
En ce qui concerne son mandat de production de rapports, le CEPMB a continué à établir des partenariats stratégiques et à sensibiliser le public à l’égard de ce mandat en améliorant la façon dont il répond aux besoins des payeurs pharmaceutiques en matière d’information tout en élargissant la portée de ses rapports pour cibler davantage d’intervenants. Un exemple de cette dernière mesure était la publication de la Veille des médicaments mis en marché dans le cadre de l’initiative du Système national d’information sur l’utilisation des médicaments prescrits (SNIUMP). Un exemple de la première mesure est le Rapport sur la situation du marché : Modificateurs de la réponse biologique du CEPMB, le premier d’une série de rapports conçus pour donner un meilleur aperçu des segments précis du marché thérapeutique qui sont importants pour les payeurs publics et privés au Canada.
Le gouvernement a augmenté de façon importante le financement du CEPMB dans le budget de 2017 en vue de respecter son engagement de rendre les médicaments sur ordonnance plus accessibles et abordables pour les Canadiens. Pour nous, cela témoigne de la confiance du gouvernement à l’égard du CEPMB dans sa capacité de jouer un rôle pertinent et important pour améliorer la durabilité du système de santé canadien. En décembre 2017, nous célébrerons le 30e anniversaire de la création du CEPMB et ce sera une occasion des plus propices pour souligner nos succès dans le passé et tourner notre regard vers un avenir très prometteur.
Dr Mitchell Levine
Aperçu de nos résultats
Dépenses réelles : 10 133 959 $
ETP réels : 63,7
Pour en savoir plus sur les plans, les priorités et les résultats du Ministère, voir la section « Résultats : ce que nous avons accompli » du présent rapport.
Mandat de réglementation
- En juin 2016, le CEPMB a lancé la Phase 1 de l’initiative de consultation Repenser les Lignes directrices au moyen de la publication de son document de discussion sur la modernisation des Lignes directrices. Le CEPMB a reçu 65 présentations de patients, de provinces, d’universitaires, d’assureurs privés, de sociétés pharmaceutiques, de professionnels de la santé et de groupes de revendication représentant plus de 500 intervenants de l’industrie pharmaceutique. En mai 2017, la ministre a annoncé son intention d’aller de l’avant avec les modifications au Règlement sur les médicaments brevetés visant à doter le CEPMB d’outils de réglementation plus pertinents et plus efficaces pour protéger les Canadiens contre les prix excessifs. Cette initiative est fondée sur les propositions écrites reçues par le CEPMB en réponse à son document de discussion publié en juin 2016.
- Le CEPMB a accepté huit engagements de conformité volontaireNotes de bas de page i qui ont entraîné des réductions de prix pour certains produits pharmaceutiques et le remboursement de recettes excédentaires totalisant 35 856 156,83 $ au moyen de paiements versés au gouvernement du Canada.
- Les conclusions finales de la première audience sur les prix excessifs tenue par le CEPMB depuis plusieurs années, qui est également la première activité de cette nature à laquelle les assureurs publics et privés ont demandé de participer, ont été présentées en avril 2017.
Mandat de rapport
- En plus du dépôt du rapport annuel de 2015 et du document de discussion sur la modernisation des Lignes directrices du CEPMB de juin 2016, le CEPMB a publié les rapports analytiques suivants :
Rapport sur la situation du marché : Modificateurs de la réponse biologique, 2015, octobre 2016
Veille des médicaments mis en marché, 2015, avril 2017
CompasRx : Rapport annuel sur les dépenses des régimes publics d’assurance-médicaments, 3e édition, mai 2017;
Raison d’être, mandat et rôle : qui nous sommes et ce que nous faisons
Raison d’être
Créé par le Parlement en 1987, le Conseil d’examen du prix des médicaments brevetés (CEPMB) est un organisme indépendant qui détient des pouvoirs quasi judiciaires. Il est investi d’un double mandat :
- Réglementaire – veiller à ce que les prix auxquels les brevetés vendent leurs médicaments brevetés au Canada ne soient pas excessifs;
- Production de rapports – sur les tendances pharmaceutiques de tous les médicaments et sur les dépenses de la recherche et le développement (R D) effectuées par les titulaires de brevets pharmaceutiques.
Dans le cadre de l’exécution de son mandat, le CEPMB veille à ce que les Canadiens soient protégés du prix excessif des médicaments brevetés vendus au Canada et à ce que les intervenants soient informés des tendances pharmaceutiques.
Mandat et rôle
Le CEPMB a été créé à la suite des modifications apportées à la Loi sur les brevets (la « Loi ») en 1987 (projet de loi C-22), et ses pouvoirs de redressement ont été complétés par d’autres modifications en 1993 (projet de loi C-91). Ces révisions s’inscrivaient dans des réformes réglementaires visant à établir un juste équilibre entre la protection des consommateurs et les mesures visant à encourager les investissements dans la recherche et le développement de la part des titulaires de brevets pharmaceutiques.
Le CEPMB est investi d’un double rôle :
Réglementation
Il incombe au CEPMB de veiller à ce que les prix départ-usine demandés par les titulaires de brevets pour les médicaments brevetés vendus au Canada, avec ou sans ordonnance, aux grossistes, aux hôpitaux ou aux pharmacies, pour usage humain ou vétérinaire, ne soient pas excessifs. Le CEPMB réglemente le prix de chaque médicament breveté auquel Santé Canada a attribué un numéro d’identification du médicament (DIN) dans le cadre de son processus d’examen des prix. Le mandat du CEPMB couvre également les médicaments distribués au titre du Programme d’accès spécial ou par l’entremise du programme d’essais cliniques de même que les drogues nouvelles de recherche. Les médicaments brevetés en vente libre et les médicaments brevetés à usage vétérinaire sont également réglementés par le CEPMB en fonction des plaintes reçues.
Rapport
Chaque année, le CEPMB rend compte au Parlement, par le truchement du ministre de la Santé, de ses activités d’analyse des prix, des prix des médicaments brevetés, des tendances des prix de l’ensemble des médicaments d’ordonnance et des dépenses en recherche et développement (R-D) déclarées par les sociétés pharmaceutiques brevetées. De plus, à la suite de l’établissement du SNIUMPNotes de bas de page ii par les ministres de la Santé fédéral, provinciaux et territoriaux (FPT) en septembre 2001, le CEPMB réalise des analyses critiques des tendances relatives aux prix, à l’utilisation et aux coûts des médicaments brevetés et non brevetés, pour que le système de santé au Canada dispose de renseignements plus complets et plus justes sur l’utilisation des médicaments d’ordonnance et les facteurs à l’origine de l’augmentation des coûts. Cette fonction a pour objet de fournir aux gouvernements FPT et à d’autres intervenants intéressés une source crédible centralisée d’information sur les tendances pharmaceutiques. De plus en plus, conformément à son mandat en matière de rapport, le CEPMB travaille en étroite collaboration avec les gouvernements provinciaux et territoriaux dans le cadre du SNIUMP et collabore directement avec les administrations responsables par l’intermédiaire du Conseil de la fédération, afin d’offrir des analyses de prix et des études de marché pertinentes visant à réduire le prix des médicaments génériques achetés par les payeurs publics au Canada.
Pour obtenir de plus amples renseignements généraux sur le Ministère, consulter la section « Renseignements supplémentaires » du présent rapport. Pour en savoir plus sur les engagements organisationnels formulés dans la lettre de mandat du Ministère, consulter la lettre de mandat du ministreNotes de bas de page iii sur le site Web du premier ministre du Canada.
Contexte opérationnel et principaux risques
Contexte opérationnel
Les médicaments d’ordonnance constituent un élément de plus en plus important du système de soins de santé. Ils contribuent à prévenir et traiter les maladies, et à sauver des vies. Cependant, les dépenses du Canada en matière de médicaments, qui sont élevées au regard des normes internationales, ne procurent pas autant d’avantages qu’elles le devraient.
Les dépenses en médicaments du Canada, qui représentaient moins de 10 % des dépenses totales en santé lorsque le régime d’assurance maladie a été mis en place, en représentent aujourd’hui 16 %. Les médicaments constituent la deuxième plus importante catégorie de dépenses de santé, devant les dépenses liées aux services des médecins, et le Canada se classe au deuxième rang, derrière les États-Unis, au chapitre des dépenses en médicaments par habitant. Le Canada paie plus cher pour les médicaments d’ordonnance que la plupart des autres pays développés, ce qui peut avoir pour conséquence de limiter l’accès à des médicaments novateurs, d’alourdir le fardeau financier des patients, et de diminuer les ressources disponibles pour d’autres secteurs cruciaux du système de soins de santé.
En janvier 2016, les ministres des gouvernements fédéral, provinciaux et territoriaux ont convenu de travailler ensemble pour rendre les médicaments d’ordonnance plus abordables et pour en accroître l’accessibilité et l’utilisation adéquate, afin de mieux répondre aux besoins du système de soins de santé. Le gouvernement fédéral est fortement résolu à mener à bien ce travail et prend des mesures afin de réduire considérablement le coût des médicaments d’ordonnance, de permettre un accès plus rapide à de nouveaux médicaments sûrs et efficaces qui répondent mieux aux besoins du système de soins de santé, et d’appuyer la mise au point d’outils permettant d’améliorer les pratiques de prescription. Le gouvernement fédéral a prévu, dans son budget de 2017, un investissement de 140,3 millions de dollars sur 5 ans à compter de 2017, et de 18,2 millions les années subséquentes, pour appuyer ces mesures. Ces fonds sont destinés à Santé Canada, au CEPMB et à l’ACMTS afin qu’ils modernisent leurs processus d’examen des produits thérapeutiques en vue d’améliorer l’accès aux médicaments d’ordonnance, de faire baisser le prix des médicaments et de favoriser les pratiques de prescription appropriées.
En mai 2017, la ministre a présenté un plan complet visant à améliorer le système pharmaceutique du Canada. Ce plan prévoit le lancement d’un processus de consultationNotes de bas de page iv sur des modifications proposées au Règlement sur les médicaments brevetés qui permettraient de réduire les coûts des médicaments d’ordonnance au Canada et de mieux protéger les Canadiens contre les prix excessifs des médicaments. Le document de discussion de Santé Canada qui décrit ces modifications réglementaires potentielles repose sur des observations écrites reçues par le CEPMB en réponse à sa récente initiative de consultation Repenser les Lignes directricesNotes de bas de page v. Compte tenu de l’interdépendance du Règlement et des Lignes directrices, le CEPMB attendra les résultats du processus de modification du Règlement avant de reprendre les consultations sur la modernisation des Lignes directrices.
Principaux risques
blank
| Risques |
Stratégie d’atténuation et efficacité |
Lien aux programmes du ministère |
Lien aux engagements de la lettre de mandat ou aux priorités pangouvernementales et ministérielles |
| Le prix des médicaments brevetés au Canada – surtout des médicaments spécialisés onéreux – risque de continuer à augmenter à des niveaux intenables pour les tiers payants publics et privés. |
- Le CEPMB modernise son cadre réglementaire en modifiant ses lignes directrices et règlements afin de disposer d’outils plus efficaces et pertinents pour protéger les Canadiens contre le prix excessif des médicaments brevetés dans le milieu pharmaceutique d’aujourd’hui.
- En juin 2016, le CEPMB a lancé des consultations sur la réforme des lignes directrices. En mai 2017, la ministre a lancé des consultations sur les modifications proposées au règlement du CEPMB.
|
Programme de réglementation du prix des médicaments brevetés |
La proposition est conforme aux priorités du gouvernement du Canada et à la lettre de mandat du ministre de la Santé et appuie le mandat de Santé Canada visant à aider les Canadiens à préserver et à améliorer leur santé.
Priorités du CEPMB :
Modernisation du cadre
|
| Le CEPMB risque d’avoir de la difficulté à attirer et à retenir les personnes ayant les compétences et l’expertise spécialisées requises pour mettre en œuvre les nouveaux facteurs de prix excessifs envisagés en vertu des modifications proposées au règlement par la ministre. |
- Le CEPMB adoptera une approche souple et pragmatique à l’égard de la dotation qui lui permettra de repérer et d’embaucher en temps opportun des personnes provenant des secteurs public et privé qui possèdent la scolarité, les antécédents et l’expérience recherchés.
|
Services internes |
La proposition est conforme à la nouvelle orientation en dotation de la CFP.
Priorités du CEPMB :
Mobilisation des employés
|
| Il y a de multiples affaires judiciaires en cours, dans le cadre desquelles on tente de remettre en question la compétence du CEPMB ou la constitutionnalité de ses dispositions habilitantes. Il y a un risque que le dénouement de ces affaires limite la compétence du CEPMB et nuise à sa capacité de remplir son mandat de protection des consommateurs. |
- Le CEPMB continuera de travailler en étroite collaboration avec le procureur général pour défendre les autres cas et tous les cas futurs afin d’atténuer tout risque que les pouvoirs en matière de protection des consommateurs soient restreints par suite d’une décision défavorable de la cour. En 2016-2017, la Cour fédérale s’est ralliée au PG concernant le rejet de deux contrôles judiciaires des décisions du CEPMB.
|
Programme de réglementation du prix des médicaments brevetés |
La proposition est conforme à l’engagement pour les médicaments d’ordonnance abordables dans la lettre de mandat du ministre de la Santé
Priorités du CEPMB :
Réglementation et rapports axés sur le consommateur
Partenariats stratégiques et sensibilisation du public
|
Au cours des vingt dernières années, le contexte mondial de l’industrie pharmaceutique a subi de nombreux changements. Deux de ces changements sont particulièrement pertinents dans le cas présent : 1) l’émergence de médicaments à coût élevé, tels que les produits biologiques et les thérapies génétiques, qui exercent une pression croissante sur les dépenses en médicaments; 2) un écart croissant entre les prix courants publics et les prix réels du marché, qui diminuent avec la multiplication des remises et des rabais confidentiels.
Ces changements ont mené d’autres pays à essayer de nouveaux moyens pour limiter les coûts, qui reposent davantage sur l’évaluation de la valeur économique des nouveaux médicaments pour leur propre système de santé que sur la comparaison des prix de ces médicaments à l’échelle internationale. L’absence d’une réforme similaire a contribué à l’augmentation des prix des médicaments brevetés au Canada, lesquels sont parmi les plus élevés au monde, et à des dépenses en médicaments relativement élevées par habitant et par rapport au PIB.
En raison de son environnement opérationnel en mutation, le CEPMB a jugé nécessaire d’étudier la nécessité d’apporter des changements connexes afin de moderniser son cadre réglementaire. Comme première étape dans ce processus, le CEPMB effectue des consultations publiques pour obtenir les observations des intervenants et du grand public au sujet des Lignes directrices. Le CEPMB a reçu 65 observations écrites de patients, de provinces, d’universitaires, d’assureurs privés, de sociétés pharmaceutiques, de professionnels de la santé et de groupes de revendication représentant plus de 500 intervenants de l’industrie pharmaceutique.
À partir des commentaires des intervenants, la ministre de la Santé a proposé, en mai 2017, un plan global afin d’améliorer le système pharmaceutique du Canada. Ce plan prévoit le lancement d’un processus de consultation sur des modifications proposées au Règlement sur les médicaments brevetés (le Règlement) qui donneraient au CEPMB des outils réglementaires améliorés permettant de réduire les coûts des médicaments d’ordonnance au Canada et de mieux protéger les Canadiens des prix excessifs des médicaments. La consultation en ligne s’est terminée le 28 juin 2017. Compte tenu de l’interdépendance du Règlement et des Lignes directrices, le CEPMB attendra les résultats du processus de consultation de Santé Canada avant de reprendre les consultations sur la modernisation des Lignes directrices.
Résultats : ce que nous avons accompli
Programmes
Programme de réglementation du prix des médicaments brevetés
Description
Le CEPMB est un organisme indépendant qui détient des pouvoirs quasi judiciaires et qui est responsable de s’assurer que les prix auxquels les brevetés vendent leurs médicaments brevetés au Canada ne sont pas excessifs en vertu des facteurs d’examen du prix prévus à la Loi sur les brevets (la Loi). Pour décider si un prix est excessif, le Conseil doit tenir compte des facteurs suivants : les prix de vente du médicament et des autres médicaments de la même catégorie thérapeutique au Canada et dans les sept pays de comparaison nommés dans le Règlement sur les médicaments brevetés (le Règlement); les variations de l’Indice des prix à la consommation (IPC); et, conformément à la Loi, tous les autres facteurs précisés par les règlements d’application visant l’examen du prixNotes de bas de page vi. En vertu de la Loi et du Règlement, les brevetés sont tenus de faire rapport des renseignements sur les prix et les ventes pour chaque médicament breveté vendu au Canada, jusqu’à échéance du brevet ou des brevets. Le personnel du Conseil examine les renseignements soumis par les brevetés au lancement et à chaque période de rapport, et ce, pour tous les médicaments brevetés vendus au Canada. S’il conclut que le prix d’un médicament breveté semble excessif, le personnel du Conseil mène une enquête sur le prix. Une enquête peut mener aux résultats suivants : la fermeture de l’enquête lorsqu’il apparaît que le prix est non excessif; un Engagement de conformité volontaire par lequel le breveté s’engage à réduire le prix de son produit et à rembourser les recettes excessives au moyen d’un paiement ou d’une réduction du prix d’un autre produit médicamenteux breveté; ou une audience publique dont l’objet est de déterminer si le prix du produit médicamenteux est ou non excessif, y compris une ordonnance corrective rendue par le Conseil. Si le comité d’audience du Conseil conclut, à l’issue d’une audience publique, qu’un prix est ou était excessif, il peut ordonner au breveté de réduire le prix et de prendre des mesures pour rembourser les recettes excessives. Ce programme assure la protection des Canadiens et de leur système des soins de santé en effectuant l’examen des prix auxquels les brevetés vendent leurs médicaments brevetés au Canada afin d’éviter les prix excessifs.
Résultats atteints
| Résultats attendus |
Indicateurs de rendement |
Cible |
Date d’atteinte de la cible |
Résultats réels
2016–2017 |
Résultats réels
2015–2016 |
Résultats réels
2014–2015 |
| La conformité des brevetés à la Loi sur les brevets, à la réglementation et aux Lignes directrices sur les prix excessifs (les « Lignes directrices ») |
Pourcentage de médicaments brevetés dont les prix sont fixés suivant les Lignes directrices, ou ne justifient pas la tenue d’une enquête, en conséquence de la conformité volontaire |
95 %Note de bas de page vii |
Le 31 mars chaque année |
92,3 %Note de bas de page viii |
93 % |
95,3 % |
| Taux de conformité aux ordonnances du Conseil relatives au prix ou à la compétence et aux engagements de conformité volontaire |
100 % |
Le 31 mars chaque année |
100 % |
100 % |
100 % |
| Prix canadiens des médicaments brevetés qui se trouvent en dessous de la moyenne du prix médian international |
50 % |
Le 31 mars chaque année |
58 % |
s/oNote de bas de page ix |
s/o |
Ressources financières budgétaires (en dollars)
blank
Budget principal des dépenses
2016-2017 |
Dépenses prévues
2016-2017 |
Autorisations totales pouvant être utilisées
2016-2017 |
Dépenses réelles (autorisations utilisées)
2016-2017 |
Écart
(dépenses réelles moins dépenses prévues)
2016-2017 |
| 6 646 758 |
6 646 758 |
6 834 705 |
6 098 659 |
(548 099) |
Ressources humaines (équivalents temps plein ou ETP)
blank
Nombre d’ETP prévus
2016-2017 |
Nombre d’ETP réels
2016-2017 |
Écart (nombre d’ETP réels moins nombre d’ETP prévus)
2016-2017 |
| 40,0 |
31,1 |
(8,9) |
La politique de conformité actuelle du CEPMB a été fondée sur le principe selon lequel le moyen le plus efficace de protéger le public contre des prix excessifs et d’atteindre le maximum de conformité est de se fier d’abord à la conformité volontaire des brevetés. Malgré le fait que le taux de conformité envers les Lignes directrices du CEPMB a constamment été élevé, les prix des médicaments brevetés au Canada ont progressivement augmenté au cours des dernières années par rapport aux prix dans le CEPMB7.
En 2016, les prix au Canada étaient résolument plus élevés que ceux pratiqués au Royaume-Uni, en France, en Italie et en Suède. En outre, comme indiqué dans le Rapport annuel 2016 du CEPMBNotes de bas de page x, les prix canadiens sont en moyenne de 20 % supérieurs aux prix médians de l’OCDE. Les prix canadiens sont les troisièmes plus élevés parmi les 31 pays de l’OCDE, derrière seulement les États-Unis et la Suisse et sur un pied d’égalité avec l’Allemagne.
Le cadre réglementaire actuel du CEPMB n’offre pas suffisamment d’outils pour relever les défis actuels et prévus sur le plan de la fixation des prix. Par exemple, au cours des dernières années, bon nombre de fabricants pharmaceutiques ont orienté leurs efforts de R-D vers des maladies plus graves touchant une petite population de patients. Les médicaments efficaces qui découlent de ce type de R et D (souvent appelés « médicaments spécialisés ») ont tendance à être vendus à des prix de plus en plus élevés afin de refléter les réalités du marché différentes en lien à la taille de la population, à l’efficacité du médicament et au manque de choix thérapeutiques ou de concurrence. Le cadre actuel, auquel aucune modification importante n’a été apportée depuis plus de deux décennies, ne tient pas compte de ces facteurs. Il ne prévoit également aucune disposition pour déterminer si le prix d’un médicament reflète sa valeur pour les patients ou la taille de son marché potentiel.
L’année 2016 a marqué le lancement de l’initiative de consultation Repenser les Lignes directrices, qui constitue une première étape clé des mesures du CEPMB pour moderniser son cadre réglementaire. La première phase de cette consultation, qui s’est déroulée de juin à octobre 2016, visait à obtenir la rétroaction des intervenants et du public au sujet du document de discussion sur la modernisation des Lignes directricesNotes de bas de page xi. Les observations écrites présentées par les parties intéressées dans le cadre de cette consultation sont affichées en ligne et les consultations dirigées par le CEPMB se poursuivront après la publication prévue, à l’automne, des modifications proposées par la ministre de la Santé au Règlement sur les médicaments brevetés dans la Partie I de la Gazette du Canada.
Le CEPMB a mené un grand nombre d’activités de conformité et d’application de la loi en 2016 en raison de sa décision de remettre l’accent sur la réglementation axée sur les consommateurs, ce qui a mené à l’acceptation de huit engagements de conformité volontaire et au remboursement de recettes excessives totalisant 35 856 156,83 $ en plus de la réduction des prix des médicaments visés. Par ailleurs, la première audience sur les prix excessifs tenue par le CEPMB en plusieurs années et la première activité de cette nature à laquelle le public ainsi que les assureurs privés ont cherché à participer s’est poursuivie au cours l’année. Elle est à l’étape des présentations sur le bien-fondé et les plaidoyers finaux devraient avoir lieu au printemps 2017.
Ce programme ne comporte pas de programmes de niveau inférieur.
Programme sur les tendances relatives aux produits pharmaceutiques
Description
Chaque année, le CEPMB rend compte au Parlement, par le truchement du ministre de la Santé, de ses activités d’analyse des prix, des prix des médicaments brevetés, des tendances des prix de l’ensemble des médicaments d’ordonnance et des dépenses en recherche et développement (R-D) déclarées par les sociétés pharmaceutiques brevetées. À l’appui de cette exigence en matière de rapport, le Programme sur les tendances relatives aux produits pharmaceutiques fournit des renseignements complets et précis sur les tendances relatives aux prix auxquels les fabricants vendent leurs médicaments brevetés au Canada et sur les dépenses de recherche-développement des brevetés aux intervenants intéressés, notamment l’industrie (c.-à-d. de médicaments d’origine, issus de la biotechnologie et génériques); les gouvernements fédéral, provinciaux et territoriaux; les groupes de défense des droits des consommateurs et des patients; les tiers payants; et autres. Ces renseignements permettent également de rassurer les Canadiens en leur démontrant que les prix des médicaments brevetés ne sont pas excessifs. De plus, à la suite de l’établissement du SNIUMP par les ministres de la Santé fédéral, provinciaux et territoriaux, la ministre fédérale de la Santé a demandé au CEPMB d’effectuer des analyses des tendances relatives au prix, à l’utilisation et aux coûts des médicaments d’ordonnance brevetés et non brevetés afin de s’assurer que le système canadien de soins de santé possède des renseignements plus exhaustifs et précis sur l’utilisation de tout médicament d’ordonnance et sur les facteurs à l’origine des augmentations de coûts. Cette fonction vise à fournir aux gouvernements fédéral, provinciaux et territoriaux ainsi qu’aux autres intervenants intéressés une source d’information centrale et fiable concernant les prix de tout médicament d’ordonnance.
Résultats atteints
| Résultats attendus |
Indicateurs de rendement |
Cible |
Date d’atteinte de la cible |
Résultats réels
2016–2017 |
Résultats réels
2015–2016 |
Résultats réels
2014–2015 |
| Information sur les tendances pharmaceutiques et les facteurs à l’origine des coûts offerte aux intervenants |
Nombre de nouveaux rapports/nouvelles études sur le site Web du CEPMB |
12 rapports et études |
Le 31 mars chaque année |
11 rapports et études |
15 rapports et études |
15 rapports et études |
| Nombre de présentations du CEPMB à un public externe |
10 séances d’information |
Le 31 mars chaque année |
21 séances d’information |
25 séances d’information |
25 séances d’information |
Ressources financières budgétaires (en dollars)
blank
Budget principal des dépenses
2016-2017 |
Dépenses prévues
2016-2017 |
Autorisations totales pouvant être utilisées
2016-2017 |
Dépenses réelles (autorisations utilisées)
2016-2017 |
Écart
(dépenses réelles moins dépenses prévues)
2016-2017 |
| 1 704 508 |
1 704 508 |
1 739 258 |
1 616 278 |
(88 230) |
Ressources humaines (équivalents temps plein ou ETP)
blank
Nombre d’ETP prévus
2016-2017 |
Nombre d’ETP réels
2016-2017 |
Écart (nombre d’ETP réels moins nombre d’ETP prévus)
2016-2017 |
| 12,0 |
13,3 |
1,3 |
En 2016-2017, le CEPMB a poursuivi ses efforts pour établir des partenariats stratégiques et sensibiliser le public à l’égard de son mandat tout en améliorant la façon dont il répond aux besoins des payeurs en matière d’information tout en élargissant la portée de ses rapports pour cibler davantage d’intervenants. Ces efforts ont notamment compris la distribution de communiqués de presse, la mise de l’accent sur des campagnes ciblées dans les médias sociaux, la mobilisation directe du public au moyen des médias sociaux et d’autres méthodes plus traditionnelles (p. ex., courriel et téléphone) et la communication avec des médias nationaux, internationaux et spécialisés, y compris CBC, CTV, Radio-Canada, La Presse, le Globe and Mail, le Toronto Star, le Journal de l’Association médicale canadienne, Benefits Canada, CBS, Bloomberg News, le Boston Globe et VICE News.
Le CEPMB a également continué de soutenir et de renforcer ses activités d’engagement liées au SNIUMP en consultant régulièrement le Comité consultatif du SNIUMP, en participant à des conférences et des comités d’intervenants, en organisant des séances d’échange d’information avec des chercheurs et en organisant des séances d’information avec des intervenants souhaitant partager les résultats des études analytiques. En 2016-2017 dans le cadre de l’initiative du SNIUMP, le CEPMB a publié deux rapports analytiques et six affiches. L’un des rapports analytiques constituait la première édition de la nouvelle publication du SNIUMP, Veille des médicaments mis en marchéNotes de bas de page xii. Il s’agira d’une publication annuelle qui explorera la dynamique de mise en marché des nouveaux médicaments au Canada et sur d’autres marchés internationaux, conçue pour informer les décideurs, les chercheurs et les patients de l’évolution de la dynamique du marché liée aux nouvelles pharmacothérapies.
L’autre document publié était le Rapport sur la situation du marché : Modificateurs de la réponse biologiqueNotes de bas de page xiii du CEPMB, la première de la série des rapports de cette nature qui sont conçus pour donner un meilleur aperçu des segments précis du marché thérapeutique qui sont importants pour les payeurs publics et privés au Canada
En plus des rapports susmentionnés, le CEPMB déposé son Rapport annuel 2015 et a publié le document de discussion sur la modernisation des Lignes directrices du CEPMB, six présentations sous forme d’affiches et la troisième édition de CompasRx : Rapport annuel sur les dépenses des régimes publics d’assurance-médicamentsNotes de bas de page xiv, mai 2017.
En outre, le SNIUMP a mené un certain nombre d’études spéciales à la demande des administrations participantes du SNIUMP.
Ce programme ne comporte pas de programmes de niveau inférieur.
Services internes
Description
Les services internes sont des groupes d’activités et de ressources connexes que le gouvernement fédéral juge être des services au soutien des besoins des programmes et nécessaires pour satisfaire aux obligations générales d’une organisation. Les Services internes renvoient aux activités et aux ressources de dix catégories de services distinctes qui soutiennent l’exécution de programmes dans l’organisation, sans égard au modèle de prestation des Services internes du ministère. Les 10 catégories de service sont : services de gestion et de surveillance, services des communications, services juridiques, services de gestion des ressources humaines, services de gestion des finances, services de gestion de l’information, services des technologies de l’information, services de gestion des biens, services de gestion du matériel et services de gestion des acquisitions.
Résultats
Ressources financières budgétaires (en dollars)
blank
Budget principal des dépenses
2016-2017 |
Dépenses prévues
2016-2017 |
Autorisations totales pouvant être utilisées
2016-2017 |
Dépenses réelles (autorisations utilisées)
2016-2017 |
Écart (dépenses réelles moins dépenses prévues)
2016-2017 |
| 2 613 842 |
2 613 842 |
2 670 837 |
2 419 022 |
(194 820) |
Ressources humaines (équivalents temps plein ou ETP)
blank
Nombre d’ETP prévus
2016-2017 |
Nombre d’ETP réels
2016-2017 |
Écart (nombre d’ETP réels moins nombre d’ETP prévus)
2016-2017 |
| 19,0 |
19,3 |
0,3 |
Dans le Plan stratégique 2015-2018, la mobilisation des employés a été établie comme l’une de quatre priorités stratégiques du CEPMB. En mars 2016, nous avons officialisé la Stratégie de mobilisation des employés, afin d’aider à orienter nos efforts pour la création et le maintien d’un milieu de travail sain, respectueux et stimulant, en favorisant l’acceptation du changement, l’efficacité des communications et la reconnaissance.
En 2016-2017, le CEPMB a continué la présentation d’une série de conférences, tenues régulièrement, qui offrent aux employés participants l’occasion de mieux connaître les questions ayant une incidence sur leur travail et leur milieu de travail par l’entremise de discussions avec des collègues, des spécialistes du secteur et des intervenants des secteurs public et privé de même que du secteur des OSBL.
Un sondage sur la mobilisation des employés a été réalisé en juin 2016 en réponse au souhait du directeur général du CEPMB de faire en sorte que les employés aient l’occasion d’exprimer leur point de vue sur la réalisation des objectifs de la direction relativement à ses engagements.
En février 2017, le CEPMB a lancé son nouveau site intranet amélioré, l’Atrium, qui fournit des outils et des mécanismes à jour pour faciliter le dialogue entre les directions générales, les gestionnaires et les employés.
En décembre 2015, le CEPMB a mis sur pied une équipe d’amélioration du milieu de travail (ÉAMT) formée d’employés de divers groupes et divers niveaux ayant joint l’équipe à titre volontaire. L’ÉAMT a pour mandat de contribuer à un changement de culture positif et à l’amélioration du milieu de travail. L’ÉAMT a donc poursuivi, pendant l’année, la mise en œuvre de la Stratégie de mobilisation du CEPMB. Les initiatives qui ont été réalisées sont notamment l’élaboration de listes de vérification pour les gestionnaires et les employés, qui permettent de s’assurer que les gestionnaires et les employés connaissent leurs responsabilités et s’en acquittent, et l’élaboration de listes de vérification d’intégration pour les gestionnaires et les employés, qui améliorent l’expérience d’accueil et d’intégration des nouveaux employés en faisant en sorte que toutes les tâches requises en vue de leur arrivée soient effectuées. Ces initiatives ont permis d’améliorer la mobilisation du CEPMB, un objectif auquel l’ÉAMT continue de contribuer.
L’année 2016-2017 était la première année du Sondage annuel auprès des fonctionnaires fédéraux (SAAFF). Les résultats du sondage indiquent que le CEPMB s’est amélioré dans tous les domaines par rapport au Sondage auprès des fonctionnaires fédéraux de 2014. Les résultats du CEPMB ont également dépassé ceux de tous les autres petits organismes et de l’ensemble de la fonction publique, et ce pour tous les indicateurs, notamment en ce qui concerne le respect en milieu de travail, la mobilisation des employés, et le bien-être en milieu de travail. Ces résultats témoignent du succès de la stratégie de mobilisation du CEPMB.
Le CEPMB continuera d’informer et de mobiliser les employés en ce qui a trait au processus de planification stratégique et de leur donner une orientation claire sur les objectifs de travail et les comportements attendus afin de promouvoir une culture de rendement élevé constant. Il mettra en œuvre une stratégie de communication interne globale pour permettre un dialogue plus structuré entre les directions générales, les gestionnaires et les employés et mettra en place des systèmes permettant aux employés d’évaluer leurs gestionnaires selon leur degré d’atteinte des objectifs en matière de mobilisation. Le CEPMB offrira également un accès à un large éventail de possibilités d’apprentissage et de perfectionnement, y compris, mais sans s’y limiter, du mentorat et des affectations de perfectionnement.
Analyse des tendances en matière de dépenses et de ressources humaines
Dépenses réelles
Graphique des tendances relatives aux dépenses du ministère
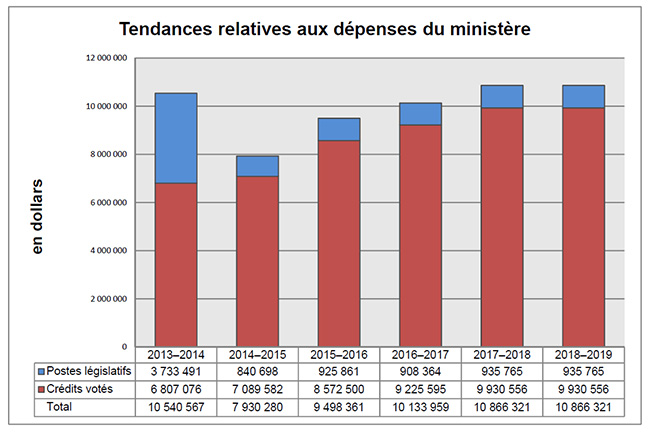
Tendances relatives aux dépenses du ministère
Le graphique à barres ci-après illustre les tendances des dépenses du CEPMB au fil du temps. Il présente les dépenses législatives et les dépenses votées réelles pour les exercices 2013-2014 à 2016-2017, ainsi que les dépenses législatives et les dépenses votées prévues pour les exercices 2017-2018 et 2018-2019.
blank
| |
2013-2014 |
2014-2015 |
2015-2016 |
2016-2017 |
2017-2018 |
2018-2019 |
| Postes législatif |
3 733 491 |
840 698 |
925 861 |
908 364 |
936 765 |
936 765 |
| Crédits votés |
6 807 076 |
7 089 582 |
8 572 500 |
9 255 595 |
9 930 556 |
9 930 556 |
| Total |
10 540 567 |
7 930 280 |
9 498 361 |
10 133 959 |
10 866 321 |
10 866 321 |
Les dépenses législatives en 2013-2014 ont été considérablement plus élevées que celles des années ultérieures, en grande partie en raison du financement supplémentaire reçu au moyen d’un mandat de rajustement pour couvrir le montant que la Cour fédérale a ordonné de rembourser à un breveté. En effet, la Cour fédérale a annulé une ordonnance du Conseil et ordonné dans sa décision qu’un revenu excédentaire de 2 801 285 $ soit remboursé par le CEPMB au breveté, avec l’intérêt approprié et les frais déterminés.
Sommaire du rendement budgétaire pour les programmes et les Services internes (en dollars)
blank
| Programmes et Services internes |
Budget principal des dépenses
2016-2017 |
Dépenses prévues
2016-2017 |
Dépenses prévues
2017-2018 |
Dépenses prévues
2018-2019 |
Autorisations totales pouvant être utilisées
2016-2017 |
Dépenses réelles (autorisations utilisées)
2016-2017 |
Dépenses réelles (autorisations utilisées)
2015-2016 |
Dépenses réelles (autorisations utilisées)
2014-2015 |
| Programme de réglementation du prix des médicaments brevetés |
6 646 758 |
a6 646 758 |
6 706 989 |
6 706 989 |
6 834 705 |
b6 098 659 |
c5 399 127 |
3 543 891 |
| Programme sur les tendances relatives aux produits pharmaceutiques |
1 704 508 |
1 704 508 |
1 575 179 |
1 575 179 |
1 739 258 |
1 616 278 |
1 688 584 |
1 301 871 |
| Total partiel |
8 351 266 |
8 351 266 |
8 282 168 |
8 282 168 |
8 573 963 |
7 714 937 |
7 087 711 |
4 845 762 |
| Services internes |
2 613 842 |
2 613 842 |
2 584 153 |
2 584 153 |
2 670 837 |
2 419 022 |
2 410 650 |
3 084 518 |
| Total |
10 965 108 |
10 965 108 |
10 866 321 |
10 866 321 |
11 244 800 |
10 133 959 |
9 498 361 |
7 930 280 |
a Le CEPMB prévoit toujours ses dépenses en se fondant sur l’hypothèse qu’il dépensera la totalité des 2,44 millions de dollars de l’ABS réservés à la tenue d’audiences publiques. La raison en est que ces dépenses dépendent du nombre d’audiences, de la durée et de la complexité des audiences qui se dérouleront, ce qui est difficile à prévoir
b Les dépenses réelles pour 2016-2017 ont été considérablement plus élevées que celles de 2015-2016. Cet écart est dû en grande partie aux dépenses de l’ABS de 1 883 221 $, dont la majorité est liée aux coûts associés à l’audience relative au prix du médicament Soliris.
c Les dépenses réelles pour 2015-2016 ont été considérablement plus élevées que celles de 2014-2015. Cet écart est dû en grande partie aux dépenses de l’ABS de 1 213 627 $, dont la majorité est liée aux coûts associés à l’audience relative au prix du médicament Soliris.
Ressources humaines réelles
Sommaire des ressources humaines pour les programmes et les Services internes
(équivalents temps plein ou ETP)
blank
| Programmes et Services internes |
Équivalents temps plein réels
2014-2015 |
Équivalents temps plein réels
2015-2016 |
Équivalents temps plein prévus
2016-2017 |
Équivalents temps plein réels
2016-2017 |
Équivalents temps plein prévus
2017-2018 |
Équivalents temps plein prévus
2018-2019 |
| Programme de réglementation du prix des médicaments brevetés |
24,7 |
31,1 |
40,0 |
31,1 |
33,0 |
33,0 |
| Programme sur les tendances relatives aux produits pharmaceutiques |
9,2 |
12,8 |
12,0 |
13,3 |
13,0 |
13,0 |
| Total partiel |
33,9 |
43,9 |
52,0 |
44,4 |
46,0 |
46,0 |
| Services internes |
22,3 |
18,6 |
19,0 |
19,3 |
20,0 |
20,0 |
| Total |
56,2 |
62,5 |
71,0 |
63,7 |
66,0 |
66,0 |
Dépenses par crédit voté
Pour obtenir de l’information sur les dépenses votées et les dépenses législatives de CEPMB, consulter les Comptes publics du Canada 2017. Notes de bas de page xv
Harmonisation des dépenses avec le cadre pangouvernemental
Harmonisation des dépenses réelles pour 2016-2017 avec le cadre pangouvernementalNotes de bas de page xvi (en dollars)
| Programme |
Secteur de dépenses |
Secteur d’activités du gouvernement du Canada |
Dépenses réelles
2016-2017 |
| Programme de réglementation du prix des médicaments brevetés |
Affaires sociales |
Des Canadiens en meilleure santé |
6 098 659 |
| Programme sur les tendances relatives aux produits pharmaceutiques |
Affaires sociales |
Des Canadiens en meilleure santé |
1 616 278 |
Total des dépenses par secteur de dépenses (en dollars)
| Secteur de dépenses |
Total des dépenses prévues |
Total des dépenses réelles |
| Affaires économiques |
|
|
| Affaires sociales |
8 282 168 |
7 714 937 |
| Affaires internationales |
|
|
| Affaires gouvernementales |
|
|
États financiers et faits saillants des états financiers
États financiers
Les états financiers [non audités] du Conseil d’examen du prix des médicaments brevetésNotes de bas de page xvii pour l’exercice se terminant le 31 mars 2017 se trouvent sur le site Web du CEPMB.
Faits saillants des états financiers
État condensé des opérations (non audité) pour l’exercice se terminant le 31 mars 2017 (en dollars)
| c |
Résultats prévus
2016-2017 |
Réels
2016-2017 |
Réels
2015-2016 |
Écart (réels
2016-2017
moins
prévus
2016-2017) |
Écart (réels
2016-2017
moins
réels
2015-2016) |
| Total des charges |
12 157 399 |
11 140 340 |
10 716 714 |
(1 017 059) |
423 626 |
| Total des revenus |
- |
9 297 |
2 265 |
9 297 |
7 032 |
| Coût de fonctionnement net avant le financement du gouvernement et les transferts |
12 157 399 |
11 131 043 |
10 714 449 |
(1 026 356) |
416 594 |
En 2016-2017, les charges du CEPMB ont totalisé 11 140 340 $, une augmentation de 423 626 $ par rapport à 2015-2016, qui s’explique principalement par ce qui suit :
- une diminution de 181 967 $ au titre des salaires et des avantages sociaux des employés;
- une augmentation de 586 168 $ au titre des services professionnels et spéciaux.
Les revenus du CEPMB, généralement constitués des frais des demandes d’accès à l’information et du produit de l’aliénation d’immobilisations et de gains de taux de change ont totalisé 9 297 $ en 2016-2017, soit une augmentation de 7 032 $ par rapport aux revenus annuels de l’exercice précédent. L’augmentation cette année s’explique principalement par l’augmentation des gains de taux de change.
État condensé de la situation financière (non audité) au 31 mars 2017 (en dollars)
| Information financière |
2016–2017 |
2015–2016 |
Écart
(2016-2017
moins
2015-2016) |
| Total des passifs nets |
2 294 983 |
1 995 264 |
299 719 |
| Total des actifs financiers nets |
1 722 674 |
1 291 599 |
431 075 |
| Dette nette du ministère |
572 309 |
703 665 |
(131 356) |
| Total des actifs non financiers |
100 895 |
155 071 |
(54 176) |
| Situation financière nette du ministère |
(471 414) |
(548 594) |
77 180 |
Le total des passifs nets du CEPMB était de 2 294 983 $ à la fin de 2016-2017, soit une augmentation de 299 719 $ par rapport à l’exercice précédent. L’augmentation comportait principalement ce qui suit :
- une augmentation de 431 075 $ au titre des créditeurs et charges à payer;
- une diminution de 41 340 $ au titre des indemnités de vacances et congés compensatoires;
- une diminution de 90 016 $ au titre des avantages sociaux futurs.
Le total des actifs du CEPMB était de 1 722 674 $ à la fin de 2016-2017, une augmentation de 431 075 $ par rapport à l’exercice précédent. Les écarts dans les actifs comportaient principalement ce qui suit :
- une augmentation de 341 286 $ au titre du montant à recevoir du Trésor;
- une augmentation de 89 789 $ au titre des débiteurs et avances.
Renseignements supplémentaires
Renseignements ministériels
Profil organisationnel
Ministre de tutelle : L’honorable Ginette Petitpas Taylor
Administrateur général : Dr Mitchell Levine, Vice-présidentNote de bas de page xviii
Portefeuille ministériel : Santé
Instruments habilitants : Loi sur les brevetsNote de bas de page xix et Règlement sur les médicaments brevetésNote de bas de page xx
Année d’incorporation ou de création : 1987
Autres : Le ministre de la Santé est responsable de l’application des dispositions de la Loi sur les brevets (la Loi) formulées aux articles 79 à 103. Même s’il fait partie du portefeuille de la Santé, le Conseil d’examen du prix des médicaments brevetés, en raison de ses responsabilités quasi judiciaires, exerce son mandat en toute indépendance vis-à-vis du ministre de la Santé. Il fonctionne également d’une façon indépendante de Santé Canada, qui autorise la vente des médicaments au Canada après avoir vérifié leur innocuité, leur efficacité et leur qualité, d’autres membres du portefeuille de la santé, comme l’Agence de la santé publique du Canada, les Instituts de recherche en santé du Canada et l’Agence canadienne d’inspection des aliments, les régimes publics fédéral, provinciaux et territoriaux d’assurance-médicaments qui autorisent l’inscription des médicaments sur leurs formulaires de médicaments admissibles à un remboursement et le Programme commun d’examen des médicaments, géré par l’Association canadienne des médicaments et des technologies de la santé (ACMTS), qui évalue l’efficience des médicaments avant leur inscription sur les formulaires des régimes publics d’assurance-médicaments participants.
Cadre de présentation de rapports
Voici les résultats stratégiques et l’architecture d’alignement des programmes de référence pour 2016-2017 du Conseil d’examen du prix des médicaments brevetés :
1. Résultat stratégique : Les médicaments brevetés ne peuvent être vendus au Canada à des prix excessifs, afin de protéger les intérêts de la population canadienne. La population canadienne est également tenue informée sur les tendances concernant les produits pharmaceutiques.
1.1 Programme : Programme de réglementation du prix des médicaments brevetés
1.2 Programme : Programme sur les tendances relatives aux produits pharmaceutiques
Services internes
Renseignements connexes sur les programmes de niveau inférieur
Le CEPMB ne comporte pas de programmes de niveau inférieur. Il n’a qu’un seul objectif stratégique, deux programmes de soutien et des services internes.
Tableaux de renseignements supplémentaires
Les tableaux de renseignements supplémentaires qui suivent sont disponibles dans le site Web du CEPMB :
Dépenses fiscales fédérales
Il est possible de recourir au régime fiscal pour atteindre des objectifs de la politique publique en appliquant des mesures spéciales, comme de faibles taux d’impôt, des exemptions, des déductions, des reports et des crédits. Le ministère des Finances Canada publie chaque année des estimations et des projections du coût de ces mesures dans le Rapport sur les dépenses fiscales fédéralesNotes de bas de page xxii. Ce rapport donne aussi des renseignements généraux détaillés sur les dépenses fiscales, y compris les descriptions, les objectifs, les renseignements historiques et les renvois aux programmes des dépenses fédéraux connexes. Les mesures fiscales présentées dans ce rapport relèvent du ministre des Finances.
Coordonnées de l’organisation
Conseil d’examen du prix des médicaments brevetés
C.P. L40
Centre Standard Life
333, avenue Laurier Ouest
Bureau 1400
Ottawa (Ontario) K1P 1C1
Téléphone : 613-952-7360
Sans frais : 1-877-861-2350
Télécopieur : 613-288-9643
AST : 613-288-9654
Courriel : pmprb@pmprb-cepmb.gc.ca
Site Web: www.pmprb-cepmb.gc.ca
Annexe : définitions
architecture d’alignement des programmes (Program Alignment Architecture)
Répertoire structuré de tous les programmes d’un ministère ou organisme qui décrit les liens hiérarchiques entre les programmes et les liens aux résultats stratégiques auxquels ils contribuent.
brevet (patent)
Instrument émis par le commissaire des brevets sous forme de lettres patentes donnant à l’inventeur un monopole pour une période limitée. Le brevet donne à son titulaire et à ses représentants légaux le droit exclusif de fabriquer, de construire, d’exploiter ou de vendre son invention.
breveté (patentee)
Aux termes du paragraphe 79(1) de la Loi sur les brevets, un « breveté » est « La personne ayant pour le moment droit à l’avantage d’un brevet pour une invention liée à un médicament, ainsi que quiconque était titulaire d’un brevet pour une telle invention ou exerce ou a exercé les droits d’un titulaire dans un cadre autre qu’une licence prorogée en vertu du paragraphe 11(1) de la Loi de 1992 modifiant la Loi sur les brevets ».
cadre ministériel des résultats (Departmental Results Framework)
Comprend les responsabilités essentielles, les résultats ministériels et les indicateurs de résultat ministériel.
cible (target)
Niveau mesurable du rendement ou du succès qu’une organisation, un programme ou une initiative prévoit atteindre dans un délai précis. Une cible peut être quantitative ou qualitative.
CEPMB7 (PMPRB7)
Les sept pays de comparaison pour lesquels les brevetés doivent faire rapport des prix de leurs produits médicamenteux brevetés accessibles au public aux fins d’examen des prix : la France, l’Allemagne, l’Italie, la Suède, la Suisse, le Royaume-Uni et les États-Unis.
crédit (appropriation)
Autorisation donnée par le Parlement d’effectuer des paiements sur le Trésor.
dépenses budgétaires (budgetary expenditures)
Dépenses de fonctionnement et en capital; paiements de transfert à d’autres ordres de gouvernement, à des organisations ou à des particuliers; et paiements à des sociétés d’État.
dépenses législatives (statutory expenditures)
Dépenses approuvées par le Parlement à la suite de l’adoption d’une loi autre qu’une loi de crédits. La loi précise les fins auxquelles peuvent servir les dépenses et les conditions dans lesquelles elles peuvent être effectuées.
dépenses non budgétaires (non-budgetary expenditures)
Recettes et décaissements nets au titre de prêts, de placements et d’avances, qui modifient la composition des actifs financiers du gouvernement du Canada.
dépenses prévues (planned spending)
En ce qui a trait aux Plans ministériels et aux Rapports sur les résultats ministériels, les dépenses prévues s’entendent des montants approuvés par le Conseil du Trésor au plus tard le 1er février. Elles peuvent donc comprendre des montants qui s’ajoutent aux dépenses prévues indiquées dans le budget principal des dépenses.
Un ministère est censé être au courant des autorisations qu’il a demandées et obtenues. La détermination des dépenses prévues relève du ministère, et ce dernier doit être en mesure de justifier les dépenses et les augmentations présentées dans son Plan ministériel et son Rapport sur les résultats ministériels.
dépenses votées (voted expenditures)
Dépenses approuvées annuellement par le Parlement dans le cadre d’une loi de crédits. Le libellé de chaque crédit énonce les conditions selon lesquelles les dépenses peuvent être effectuées.
équivalent temps plein (full-time equivalent)
Mesure utilisée pour représenter une année-personne complète d’un employé dans le budget ministériel. Les équivalents temps plein sont calculés par un rapport entre les heures de travail assignées et les heures de travail prévues. Les heures normales sont établies dans les conventions collectives.
évaluation (evaluation) :
Au sein du gouvernement du Canada, collecte et analyse systématiques et neutres de données probantes en vue d’évaluer le bien-fondé, le mérite ou la valeur. L’évaluation guide la prise de décisions, les améliorations, l’innovation et la reddition de comptes. Elle porte habituellement sur les programmes, les politiques et les priorités et examine des questions se rapportant à la pertinence, à l’efficacité et à l’efficience. Toutefois, selon les besoins de l’utilisateur, l’évaluation peut aussi examiner d’autres unités, thèmes et enjeux, notamment des solutions de rechange aux interventions existantes. L’évaluation utilise généralement des méthodes de recherche des sciences sociales.
indicateur de rendement (performance indicator)
Moyen qualitatif ou quantitatif de mesurer un extrant ou un résultat en vue de déterminer le rendement d’une organisation, d’un programme, d’une politique ou d’une initiative par rapport aux résultats attendus.
indicateur de résultat ministériel (Departmental Result Indicator)
Facteur ou variable qui présente une façon valide et fiable de mesurer ou de décrire les progrès réalisés par rapport à un résultat ministériel.
initiative horizontale (horizontal initiatives)
Initiative dans le cadre de laquelle au moins deux organisations fédérales, par l’intermédiaire d’une entente de financement approuvée, s’efforcent d’atteindre des résultats communs définis, et qui a été désignée (par exemple, par le Cabinet ou par un organisme central, entre autres) comme une initiative horizontale aux fins de gestion et de présentation de rapports.
médicament (medicine)
Toute substance ou tout mélange de substances, qui peut avoir été produit biologiquement, chimiquement ou autrement, qui est appliqué ou administré in vivo à des humains ou des animaux pour faciliter le diagnostic, le traitement l’atténuation ou la prévention d’une maladie, de symptômes, de troubles ou d’états physiques anormaux, ou pour modifier les fonctions organiques chez les humains ou les animaux. Pour être plus précis, cette définition comprend les vaccins, les préparations topiques, les anesthésiques et les produits diagnostiques utilisés in vivo, quel que soit le mode d’administration (p. ex., préparations transdermiques, capsules, solutions injectables, inhalatrices, etc.) Cette définition exclut toutefois les appareils médicaux, les produits diagnostiques in vitro et les désinfectants qui ne sont pas utilisés in vivo.
plan (plans)
Exposé des choix stratégiques qui montre comment une organisation entend réaliser ses priorités et obtenir les résultats connexes. De façon générale, un plan explique la logique qui sous-tend les stratégies retenues et tend à mettre l’accent sur des mesures qui se traduisent par des résultats attendus.
Plan ministériel (Departmental Plan)
Fournit les renseignements sur les plans et le rendement attendu des ministères appropriés au cours d’une période de trois ans. Les Plans ministériels sont présentés au Parlement au printemps.
priorité (priorities)
Plan ou projet qu’une organisation a choisi de cibler et dont elle rendra compte au cours de la période de planification. Il s’agit de ce qui importe le plus ou qui doit être fait en premier pour appuyer la réalisation du ou des résultats stratégiques souhaités.
priorités pangouvernementales (government-wide priorities)
Aux fins du Rapport sur les résultats ministériels 2016-2017, les priorités pangouvernementales sont des thèmes de haut niveau qui présentent le programme du gouvernement issu du discours du Trône de 2015, notamment : la croissance de la classe moyenne, un gouvernement ouvert et transparent, un environnement sain et une économie forte, la diversité en tant que force du Canada, ainsi que la sécurité et les possibilités).
production de rapports sur le rendement (performance reporting)
Processus de communication d’information sur le rendement fondée sur des éléments probants. La production de rapports sur le rendement appuie la prise de décisions, la responsabilisation et la transparence.
produit médicamenteux (drug product)
Présentation particulière d’un médicament telle que la forme posologique et la concentration de l’ingrédient actif.
programme (program)
Groupe d’intrants constitué de ressources et d’activités connexes qui est géré pour répondre à des besoins précis et pour obtenir les résultats visés, et qui est traité comme une unité budgétaire.
programme temporisé (sunset program)
Programme ayant une durée fixe et dont le financement et l’autorisation politique ne sont pas permanents. Lorsqu’un tel programme arrive à échéance, une décision doit être prise quant à son maintien. Dans le cas d’un renouvellement, la décision précise la portée, le niveau de financement et la durée.
Rapport sur les résultats ministériels (Departmental Results Report)
Présente de l’information sur les réalisations réelles par rapport aux plans, aux priorités et aux résultats attendus énoncés dans le Plan ministériel correspondant.