Conseil d’examen du prix des médicaments brevetés
L’honorable Ginette Petitpas Taylor
Ministre de la Santé
ISSN 2561-0740
Table des matières
Message du président
Aperçu de nos résultats
Raison d’être, mandat et rôle : composition et responsabilités
Contexte opérationnel et principaux risques
Résultats : ce que nous avons accompli
Analyse des tendances en matière de dépenses et de ressources humaines
Renseignements supplémentaires
Annexe : définitions
Notes en fin d’ouvrage
Message du président
J’ai le plaisir de présenter le Rapport sur les résultats ministériels 2017-2018 du Conseil d’examen du prix des médicaments brevetés (CEPMB).
Le CEPMB est un organisme administratif quasi judiciaire indépendant dont le mandat vise à protéger les consommateurs des médicaments brevetés de prix jugés excessifs et à faire rapport aux Canadiens des tendances relatives aux prix de tous les médicaments ainsi qu’aux dépenses des titulaires de brevets dans la recherche et le développement au Canada.
En 2017-2018, la principale priorité du CEPMB était de continuer de faire progresser les efforts visant à moderniser son cadre réglementaire. En décembre 2017, les modifications proposées par Santé Canada relativement au Règlement sur les médicaments brevetés (le Règlement) ont été publiées dans la partie I de la Gazette du Canada. Le Règlement constitue un produit à livrer clé pour la ministre de la Santé dans le contexte des efforts soutenus qu’elle déploie afin d’améliorer pour les patients l’accès aux médicaments d’ordonnance essentiels, notamment en les rendant plus abordables. Si elles sont adoptées, elles obligeraient le CEPMB à tenir compte de facteurs autres que les listes de prix nationales et internationales dans l’exécution de ses obligations réglementaires. Au cours du même mois, le CEPMB a publié un document d’orientation qui donne un aperçu des changements qui pourraient être apportés à ses Lignes directrices afin de rendre le Règlement opérationnel et d’appuyer notre objectif d’adopter une approche axée sur le risque pour la réglementation des prix des médicaments brevetés.
Le CEPMB a mené un grand nombre d’activités de conformité et d’application de la loi en 2017-2018 en raison de sa décision de remettre l’accent sur la réglementation axée sur les consommateurs, ce qui a mené à l’acceptation de 17 engagements de conformité volontaire et au remboursement de recettes excessives totalisant 4 229 878,65 $, en plus de la réduction des prix des médicaments visés. Outre ces initiatives de réforme réglementaire, en septembre, l’affaire Alexion a donné lieu à la première décision sur le bien-fondé de la participation du personnel du Conseil à une audience sur les prix excessifs depuis 2012.
En ce qui concerne son mandat de production de rapports, le CEPMB a continué à établir des partenariats stratégiques et à sensibiliser le public à l’égard de ce mandat (1) en améliorant la façon dont il répond aux besoins particuliers des payeurs pharmaceutiques en matière d’information tout en (2) élargissant la portée de ses rapports pour cibler davantage d’intervenants. Un exemple de la première mesure est l’édition de 2016 de la série de rapports intitulée Générique360 - Médicaments génériques au Canada du Système national d’information sur l’utilisation des médicaments prescrits (SNIUMP), qui fait état des dernières tendances en matière de ventes, d’utilisation et d’établissement des prix des médicaments génériques dans un contexte international. Un exemple de la deuxième mesure est la publication du premier rapport d’une nouvelle série en trois parties qui fait la comparaison de la couverture des régimes provinciaux et fédéral d’assurance-médicaments, Concordance des listes de médicaments des régimes publics au Canada – Partie 1 : Aperçu général. Les représentants du CEPMB ont également participé à de nombreuses conférences et autres événements publics à titre de conférenciers, de présentateurs ou d’experts-conseil et organisé des séances d’information avec des intervenants souhaitant partager les résultats des études analytiques.
Pour ce qui est des services internes, en 2017-2018, le CEPMB a pris des mesures pour transformer certains de ses services de soutien opérationnel. Notamment, on a simplifié les processus de gestion de l’information et de gestion des ressources humaines et réduit le fardeau administratif. Entre autres avantages, ces changements faciliteront grandement le processus d’embauche du personnel supplémentaire dont le CEPMB aura besoin pour appuyer sa nouvelle approche réglementaire.
Nous sommes heureux à l’idée de travailler avec tous nos intervenants alors que le CEPMB s’oriente vers une approche moderne et axée sur le risque en matière de réglementation des prix des médicaments brevetés.
Dr Mitchell Levine
Aperçu de nos résultats
Pour en savoir plus sur les plans, les priorités et les résultats atteints du Conseil d’examen du prix des médicaments brevetés (CEPMB), consulter la section « Résultats : ce que nous avons accompli » du présent rapport.
Priorité no 1 – Réglementation et rapports axés sur le consommateur
Dans le cadre de son mandat de réglementation, le CEPMB s’assure que les médicaments brevetés ne sont pas vendus au Canada à des prix excessifs. En axant ses ressources d’application de la loi sur les affaires pouvant avoir une valeur jurisprudentielle et sur celles dans lesquelles les payeurs n’ont pas de pouvoir compensatoire, en 2017-2018, le président du CEPMB a accepté 17 engagements de conformité volontaireNotes de bas de page i portant sur le prix de 24 médicaments brevetés. En 30 ans d’histoire, il s’agit du plus grand nombre d’engagements au cours d’une même année. Le mandat en matière de production de rapports qu’a le Conseil consiste à fournir aux intervenants des renseignements sur les tendances de l’industrie pharmaceutique. En 2017-2018, le Conseil a publié le premier rapport d’une série de trois faisant l’analyse des lacunes et des chevauchements au sein des régimes provinciaux et fédéral d’assurance-médicaments.
Priorité no 2 – Modernisation du cadre
En décembre 2017, après la prépublication des modifications proposées par Santé Canada au Règlement dans la Partie I de la Gazette du Canada, le CEPMB a publié un document d’orientation contenant un aperçu général de la façon dont il pourrait mettre en œuvre les modifications réglementaires au moyen de lignes directrices non exécutoires. Des consultations sur les détails du cadre décrit dans le document d’orientation auront lieu au cours de l’été 2018, en vue de la mise en œuvre d’un régime de réglementation moderne et simplifié en 2019.
Priorité no 3 – Partenariats stratégiques et sensibilisation du public
Le CEPMB a continué d’appuyer son mandat et son programme de modernisation en participant à d’innombrables conférences et comités d’intervenants, en organisant des séances d’information avec les intervenants intéressés pour leur transmettre des renseignements sur ses travaux et en consultant régulièrement le Comité consultatif du Système national d’information sur l’utilisation des médicaments prescrits (SNIUMP) sur des sujets d’intérêt en vue de la réalisation d’études analytiques.
Raison d’être, mandat et rôle : composition et responsabilités
Raison d’être
Créé par le Parlement en 1987, le CEPMB est un organisme indépendant qui détient des pouvoirs quasi judiciaires. Il est investi d’un double mandat :
- Réglementaire – veiller à ce que les prix auxquels les brevetés vendent leurs médicaments brevetés au Canada ne soient pas excessifs;
- Production de rapports – sur les tendances pharmaceutiques de tous les médicaments et sur les dépenses de la recherche et le développement (R-D) effectuées par les titulaires de brevets pharmaceutiques.
Dans le cadre de l’exécution de son mandat, le CEPMB veille à ce que les Canadiens soient protégés du prix excessif des médicaments brevetés vendus au Canada et à ce que les intervenants soient informés des tendances pharmaceutiques.
Mandat et rôle
Le CEPMB a été créé à la suite des modifications apportées à la Loi sur les brevets (la « Loi ») en 1987 (projet de loi C-22), et ses pouvoirs de redressement ont été complétés par d’autres modifications en 1993 (projet de loi C-91). Ces révisions s’inscrivaient dans des réformes réglementaires visant à établir un juste équilibre entre la protection des consommateurs et les mesures visant à encourager les investissements dans la recherche et le développement de la part des titulaires de brevets pharmaceutiques.
Le CEPMB est investi d’un double rôle :
Réglementation
Il incombe au CEPMB de veiller à ce que les prix départ-usine demandés par les titulaires de brevets pour les médicaments brevetés vendus au Canada, avec ou sans ordonnance, aux grossistes, aux hôpitaux ou aux pharmacies, pour usage humain ou vétérinaire, ne soient pas excessifs. Le CEPMB réglemente le prix de chaque médicament breveté auquel Santé Canada a attribué un numéro d’identification du médicament (DIN) dans le cadre de son processus d’examen des prix. Le mandat du CEPMB couvre également les médicaments distribués au titre du Programme d’accès spécial ou par l’entremise du programme d’essais cliniques de même que les drogues nouvelles de recherche. Les médicaments brevetés en vente libre et les médicaments brevetés à usage vétérinaire sont également réglementés par le CEPMB en fonction des plaintes reçues.
Rapport
Chaque année, le CEPMB rend compte au Parlement, par le truchement du ministre de la Santé, de ses activités d’analyse des prix, des prix des médicaments brevetés, des tendances des prix de l’ensemble des médicaments d’ordonnance et des dépenses en recherche et développement (R-D) déclarées par les sociétés pharmaceutiques brevetées. De plus, à la suite de l’établissement du SNIUMPNotes de bas de page ii par les ministres de la Santé fédéral, provinciaux et territoriaux (FPT) en septembre 2001, le CEPMB réalise des analyses critiques des tendances relatives aux prix, à l’utilisation et aux coûts des médicaments brevetés et non brevetés, pour que le système de santé au Canada dispose de renseignements plus complets et plus justes sur l’utilisation des médicaments d’ordonnance et les facteurs à l’origine de l’augmentation des coûts. Cette fonction a pour objet de fournir aux gouvernements FPT et à d’autres intervenants intéressés une source crédible centralisée d’information sur les tendances pharmaceutiques. De plus en plus, conformément à son mandat en matière de rapport, le CEPMB travaille en étroite collaboration avec les gouvernements provinciaux et territoriaux dans le cadre du SNIUMP et collabore directement avec les administrations responsables par l’intermédiaire du Conseil de la fédération, afin d’offrir des analyses de prix et des études de marché pertinentes visant à réduire le prix des médicaments génériques achetés par les payeurs publics au Canada.
Pour de plus amples renseignements généraux au sujet du Ministère, consulter la section « Renseignements supplémentaires » du présent rapport. Pour plus de renseignements sur les engagements organisationnels formulés dans la lettre de mandat du Ministère, consulter la lettre de mandat du ministreNotes de bas de page iii.
Contexte opérationnel et principaux risques
Contexte opérationnel
Il y a trente ans, le CEPMB a été créé dans le but de protéger les consommateurs en s’assurant que les prix auxquels les brevetés vendent leurs médicaments brevetés au Canada ne sont pas excessifs. Bien que le mandat du CEPMB n’ait pas changé depuis, de nombreux aspects de son environnement opérationnel ont changé de façon significative.
Les dépenses en médicaments au Canada ont augmenté, passant de moins de 6 % des dépenses totales en santé, au moment de la création du régime d’assurance-maladie, à environ 16 % en 2018. Les médicaments sont maintenant la deuxième catégorie en importance pour les dépenses en soins de santé au Canada, devant les services médicaux, les dépenses par habitant en médicaments se classant au deuxième rang derrière les États-Unis. Le Canada paie plus cher pour les médicaments d’ordonnance que la plupart des autres pays industrialisés, ce qui peut avoir pour conséquence de limiter l’accès à des médicaments novateurs, d’alourdir le fardeau financier des patients, et de diminuer les ressources disponibles pour d’autres secteurs importants du domaine des soins de santé.
Les prix des médicaments brevetés au Canada sont, en moyenne, environ 19 % plus élevés que la moyenne de l’OCDE (Organisation de coopération et de développement économiques). Cela s’explique en partie par les limites du cadre de réglementation des prix des médicaments brevetés désuet du Canada, qui évalue les prix canadiens par rapport aux listes de prix des pays où les prix des médicaments sont parmi les plus élevés au monde (France, Allemagne, Italie, Suède, Suisse, Royaume-Uni et États-Unis – que l’on appelle aussi le « CEPMB7 »).
Le cadre de réglementation des prix du CEPMB n’est pas en mesure de relever les défis actuels et futurs en matière de prix, en particulier ceux associés aux médicaments spécialisés à coût élevé. Dans le budget de 2017, le gouvernement a annoncé une augmentation substantielle du financement du CEPMB dans le cadre de son engagement à rendre les médicaments d’ordonnance plus accessibles et abordables pour les Canadiens. En décembre 2017, les modifications proposées par Santé Canada au Règlement ont été publiées dans la Partie 1 de la Gazette du Canada. Le Règlement est un produit livrable important pour la ministre de la Santé dans ses efforts continus pour améliorer l’accès des patients aux médicaments d’ordonnance nécessaires, y compris en les rendant plus abordables. Plus tard au cours du même mois, le CEPMB a publié un document d’orientation qui décrit les changements qui pourraient être apportés à ses Lignes directrices afin d’opérationnaliser le nouveau Règlement et d’appuyer l’adoption par le CEPMB d’une approche de réglementation des prix axée sur le risque qui permettrait de réduire les prix des médicaments brevetés au Canada.
Principaux risques
blank
| Risques |
Stratégie d’atténuation et efficacité |
Lien aux programmes du Ministère |
Lien aux engagements de la lettre de mandat et aux priorités pangouvernementales et ministérielles |
|
Réaliser des progrès pour rendre les médicaments brevetés plus abordables.
La modernisation du cadre réglementaire du CEPMB risque d’être retardée, et le CEPMB pourrait ne pas être en mesure de mettre en œuvre dans les délais prévus les nouveaux facteurs relatifs aux prix excessifs envisagés dans le cadre des modifications proposées par la ministre à la réglementation. |
Le CEPMB continue de travailler avec Santé Canada sur les modifications qu’il propose d’apporter au Règlement sur les médicaments brevetés :
- Décembre 2017 : Les modifications proposées par Santé Canada au Règlement sur les médicaments brevetés ont été publiées dans la Partie 1 de la Gazette du Canada.
- Par la suite, toujours en décembre, le CEPMB a publié un document d’orientation qui donne un aperçu des modifications qui pourraient être apportées à ses Lignes directrices afin de rendre le Règlement opérationnel.
- Été et automne 2018, le CEPMB tiendra des consultations ciblées avec les intervenants sur les principales modalités techniques et opérationnelles du nouveau régime.
- En cas de retard imprévu dans le processus de modification réglementaire, le CEPMB évaluera la situation et prendra les mesures qui s’imposent.
|
Programme de réglementation du prix des médicaments brevetés |
Engagement dans la lettre de mandat de la ministre de la Santé : médicaments d’ordonnance abordables
Priorité du CEPMB :
modernisation du cadre
|
|
Se doter d’une infrastructure, et la conserver, et embaucher du personnel pour moderniser le cadre
Il y a un risque que le CEPMB ne soit pas en mesure d’attirer et de maintenir en poste des personnes possédant les compétences et l’expertise nécessaires ou de disposer de locaux à bureaux adéquats pour les recevoir, ce qui retarderait sa capacité de mettre en œuvre le nouveau cadre réglementaire. |
Le CEPMB :
- a établi des réunions régulières avec les gestionnaires pour se pencher de façon proactive sur leurs besoins et renforcer la planification des ressources humaines, afin de permettre au CEPMB de trouver et d’embaucher des personnes des secteurs public et privé possédant la formation, les antécédents et l’expérience nécessaires en temps opportun.
- a créé un plan détaillé pour la transformation des locaux et un processus de surveillance pour veiller à ce que les changements ou les retards soient identifiés tôt et que des mesures correctives soient prises pour aménager suffisamment d’espace pour accueillir les employés.
|
Programme de réglementation du prix des médicaments brevetés
Programme sur les tendances relatives aux produits pharmaceutiques |
Engagement dans la lettre de mandat de la ministre de la Santé : médicaments d’ordonnance abordables
Priorité du CEPMB :
Modernisation du cadre |
Santé Canada est le principal responsable de l’avancement des modifications proposées au Règlement. Tout retard dans le processus de modification réglementaire aura une incidence sur la capacité du CEPMB à aller de l’avant avec la modification de ses Lignes directrices, de sorte que les Canadiens n’auront peut-être pas accès à des médicaments brevetés à des prix plus abordables pendant une durée prolongée. Le CEPMB continue de travailler en étroite collaboration avec Santé Canada afin de fournir tout le soutien technique et analytique nécessaire pour s’assurer que les modifications réglementaires sont finalisées dans les délais prévus. Si le Règlement n’est pas adopté sous sa forme actuelle ou s’il est retardé pour une durée indéterminée, le CEPMB élaborera des plans d’urgence pour aller de l’avant avec la réforme des Lignes directrices, conformément à son document de travail de 2016 sur la modernisation des Lignes directrices.
Quoi qu’il en soit, le CEPMB exigera un plus grand nombre d’agents de réglementation pour faire face à l’augmentation du travail d’enquête qui résultera des changements apportés aux Lignes directrices, une capacité juridique accrue pour gérer un plus grand nombre d’audiences, une plus grande expertise en économie et en épidémiologie de la santé et une infrastructure de TI plus moderne et plus conviviale. Étant donné la rareté relative de certaines des compétences recherchées par le CEPMB, il se peut que les processus de dotation nécessaires à l’arrivée des nouveaux employés requis soient retardés. Pour s’assurer d’avoir accès aux compétences voulues dans les délais prévus, le CEPMB aura recours à tous les arrangements temporaires possibles avec des experts externes. Par ailleurs, si le CEPMB réussit à attirer et à embaucher de nouveaux employés selon le calendrier actuellement prévu, il se peut qu’il n’ait pas suffisamment d’espace de bureau pour les accueillir. Le CEPMB a élaboré un plan détaillé pour remédier au manque de locaux, qui comprend l’utilisation d’un régime de travail flexible et l’utilisation de locaux à bureaux temporairement vacants ou inutilisés.
Résultats : ce que nous avons accompli
Programmes
Programme de réglementation du prix des médicaments brevetés
Description
Le CEPMB est un organisme indépendant qui détient des pouvoirs quasi judiciaires et qui est responsable de s’assurer que les prix auxquels les brevetés vendent leurs médicaments brevetés au Canada ne sont pas excessifs en vertu des facteurs d’examen du prix prévus à la Loi sur les brevets (la Loi). Pour décider si un prix est excessif, le Conseil doit tenir compte des facteurs suivants : les prix de vente du médicament et des autres médicaments de la même catégorie thérapeutique au Canada et dans les sept pays de comparaison nommés dans le Règlement sur les médicaments brevetés (le Règlement); les variations de l’Indice des prix à la consommation (IPC); et, conformément à la Loi, tous les autres facteurs précisés par les règlements d’application visant l’examen du prixNotes de bas de page iv. En vertu de la Loi et du Règlement, les brevetés sont tenus de faire rapport des renseignements sur les prix et les ventes pour chaque médicament breveté vendu au Canada, jusqu’à échéance du brevet ou des brevets. Le personnel du Conseil examine les renseignements soumis par les brevetés au lancement et à chaque période de rapport, et ce, pour tous les médicaments brevetés vendus au Canada. S’il conclut que le prix d’un médicament breveté semble excessif, le personnel du Conseil mène une enquête sur le prix. Une enquête peut mener aux résultats suivants : la fermeture de l’enquête lorsqu’il apparaît que le prix est non excessif; un engagement de conformité volontaire par lequel le breveté s’engage à réduire le prix de son produit et à rembourser les recettes excessives au moyen d’un paiement ou d’une réduction du prix d’un autre médicament breveté; ou une audience publique dont l’objet est de déterminer si le prix du médicament est ou non excessif, y compris une ordonnance corrective rendue par le Conseil. Si le panel d’audience du Conseil conclut, à l’issue d’une audience publique, qu’un prix est ou était excessif, il peut ordonner au breveté de réduire le prix et de prendre des mesures pour rembourser les recettes excessives. Ce programme assure la protection des Canadiens et de leur système des soins de santé en effectuant l’examen des prix auxquels les brevetés vendent leurs médicaments brevetés au Canada afin d’éviter les prix excessifs.
Résultats
Résultats atteints
| Résultats attendus |
Indicateurs de rendement |
Cible |
Date d’atteinte de la cible |
Résultats réels
2017-2018 |
Résultats réels
2016-2017 |
Résultats réels
2015-2016 |
| La conformité des brevetés à la Loi sur les brevets, à la réglementation et aux Lignes directrices sur les prix excessifs
(les « Lignes directrices ») |
Pourcentage de médicaments brevetés dont les prix sont fixés suivant les Lignes directrices, ou ne justifient pas la tenue d’une enquête, en conséquence de la conformité volontaire |
95 %Notes de bas de page 1 |
Le 31 mars chaque année |
91,0 %Notes de bas de page 2 |
92,3 %Notes de bas de page 3 |
93 % |
| Taux de conformité aux ordonnances du Conseil relatives au prix ou à la compétence et aux engagements de conformité volontaire |
100 % |
Le 31 mars chaque année |
100 % |
100 % |
100 % |
| Prix canadiens des médicaments brevetés qui se trouvent en dessous de la moyenne du prix médian international |
50 %Notes de bas de page 4 |
Le 31 mars chaque année |
56,4 %Notes de bas de page 5 |
58 % |
s/oNotes de bas de page 6 |
Ressources financières budgétaires (en dollars)
Budget principal des dépenses
2017-2018 |
Dépenses prévues
2017-2018 |
Autorisations totales pouvant être utilisées
2017-2018 |
Dépenses réelles (autorisations utilisées)
2017-2018 |
Écart (dépenses réelles moins dépenses prévues)
2017 2018 |
| 6 706 989 |
6 706 989 |
7 189 268 |
5 611 178 |
(1 095 811) |
Ressources humaines (équivalents temps plein)
Nombre d’équivalents temps plein prévus
2017-2018 |
Nombre d’équivalents temps plein réels
2017-2018 |
Écart (nombre d’équivalents temps plein réels moins nombre d’équivalents temps plein prévus)
2017-2018 |
| 33,0 |
30,7 |
(2,3) |
La Politique de conformité du CEPMB repose sur le principe que la façon la plus efficace et la plus efficiente de protéger le public contre les prix excessifs et d’assurer une conformité maximale est de compter principalement sur l’action volontaire des titulaires de brevets. L’importance renouvelée accordée par le CEPMB à une réglementation axée sur le consommateur s’est traduite, une fois de plus, par une année bien remplie d’activités de conformité et d’application de la loi. En 2017-2018, le président a accepté 17 engagements de conformité volontaire portant sur les prix de 24 médicaments brevetés. Ces engagements ont donné lieu à des réductions de prix pour les médicaments visés et au remboursement des recettes excessives, qui totalisaient 4 229 878,65 $.
Bien que le CEPMB ait connu un haut taux de conformité à ses Lignes directrices dans le passé, ce taux de conformité a diminué au cours des dernières années, et les prix des médicaments brevetés au Canada ont augmenté de façon constante par rapport aux prix au sein du CEPMB7. On s’attend à ce que les changements prévus pour opérationnaliser les modifications au Règlement proposées par Santé Canada pour rendre les médicaments brevetés plus abordables pour les Canadiens entraînent d’abord une augmentation des cas de non-conformité, alors que les titulaires de brevets et le personnel du CEPMB suivront le processus de changement. À ce moment-là, le CEPMB examinera la pertinence de cet indicateur et les résultats escomptés.
En 2017, les prix canadiens étaient supérieurs aux prix observés en France, en Suède, en Italie et au Royaume-Uni. De plus, comme l’indique le Rapport annuel 2017 du CEPMBNotes de bas de page v, les prix canadiens se situent en moyenne à 19 % au-dessus de la médiane des prix de l’OCDE, ce qui représente une légère diminution par rapport aux prix de 2016 (20 %). Les prix canadiens se classent au troisième rang parmi les 31 pays de l’OCDE, derrière les États-Unis et la Suisse.
En 2017-2018, Santé Canada a tenu des consultations sur un projet de mise à jour complète du Règlement afin de réduire les prix excessifs des médicaments, d’assurer la viabilité à long terme et d’harmoniser les politiques canadiennes d’établissement des prix des médicaments avec celles des pays aux vues similaires. La période de commentaires sur les modifications proposées étant terminée, et en prévision de la publication finale des modifications dans la Partie II de la Gazette du Canada, le CEPMB a repris son initiative parallèle de modernisation de ses Lignes directrices en tenant des consultations sur les modifications potentielles de ses Lignes directrices. Ces changements visent à moderniser la façon dont le CEPMB s’acquitte de son mandat qui consiste à protéger les Canadiens contre les prix excessifs des médicaments brevetés. Deux types principaux de changements sont envisagés. Dans le premier cas, les modifications réglementaires de Santé Canada visaient à rendre les médicaments d’ordonnance plus abordables. Le deuxième permettrait au CEPMB d’utiliser plus efficacement ses ressources en adoptant une approche de réglementation des prix fondée sur le risque.
À cette fin, en juin 2018, le CEPMB tiendra des consultations ciblées auprès des intervenants afin d’obtenir leurs commentaires sur les principales modalités techniques et opérationnelles des nouvelles Lignes directrices qui concrétiseraient ces changements. Ces travaux orienteront la publication de la version préliminaire des lignes directrices en vue d’une consultation publique plus large à l’automne. Le parachèvement des Lignes directrices suivra la publication finale dans la Gazette du Canada des modifications au Règlement afin de tenir compte de la possibilité que des changements soient apportés entre la prépublication et la publication finale, ce qui nécessiterait des ajustements à l’approche opérationnelle du CEPMB.
Ce programme ne comporte aucun programme de niveau inférieur.
Programme sur les tendances relatives aux produits pharmaceutiques
Description
Chaque année, le CEPMB rend compte au Parlement, par le truchement du ministre de la Santé, de ses activités d’analyse des prix, des prix des médicaments brevetés, des tendances des prix de l’ensemble des médicaments d’ordonnance et des dépenses en recherche et développement (R-D) déclarées par les sociétés pharmaceutiques brevetées. À l’appui de cette exigence en matière de rapport, le Programme sur les tendances relatives aux produits pharmaceutiques fournit des renseignements complets et précis sur les tendances relatives aux prix auxquels les fabricants vendent leurs médicaments brevetés au Canada et sur les dépenses de recherche-développement des brevetés aux intervenants intéressés, notamment l’industrie (c.-à-d. de médicaments d’origine, issus de la biotechnologie et génériques); les gouvernements fédéral, provinciaux et territoriaux; les groupes de défense des droits des consommateurs et des patients; les tiers payants; et autres. Ces renseignements permettent également de rassurer les Canadiens en leur démontrant que les prix des médicaments brevetés ne sont pas excessifs. De plus, à la suite de l’établissement du SNIUMP par les ministres de la Santé fédéral, provinciaux et territoriaux, la ministre fédérale de la Santé a demandé au CEPMB d’effectuer des analyses des tendances relatives au prix, à l’utilisation et aux coûts des médicaments d’ordonnance brevetés et non brevetés afin de s’assurer que le système canadien de soins de santé possède des renseignements plus exhaustifs et précis sur l’utilisation de tout médicament d’ordonnance et sur les facteurs à l’origine des augmentations de coûts. Cette fonction vise à fournir aux gouvernements fédéral, provinciaux et territoriaux ainsi qu’aux autres intervenants intéressés une source d’information centrale et fiable concernant les prix de tout médicament d’ordonnance.
Résultats
Résultats atteints
| Résultats attendus |
Indicateurs de rendement |
Cible |
Date d’atteinte de la cible |
Résultats réels
2017-2018 |
Résultats réels
2016-2017 |
Résultats réels
2015-2016 |
| Information sur les tendances pharmaceutiques et les facteurs à l’origine des coûts offerte aux intervenants |
Nombre de nouveaux rapports/nouvelles études sur le site Web du CEPMB |
12 rapports et études |
Le 31 mars chaque année |
12 rapports et études |
11 rapports et études |
15 rapports et études |
| Nombre de présentations du CEPMB à un public externe |
10 séances d’information |
Le 31 mars chaque année |
20 séances d’information |
21 séances d’information |
25 séances d’information |
Ressources financières budgétaires (en dollars)
Budget principal des dépenses
2017-2018 |
Dépenses prévues
2017-2018 |
Autorisations totales pouvant être utilisées
2017-2018 |
Dépenses réelles (autorisations utilisées)
2017-2018 |
Écart (dépenses réelles moins dépenses prévues)
2017-2018 |
| 1 575 179 |
1 575 179 |
1 547 082 |
1 498 746 |
(76 433) |
Ressources humaines (équivalents temps plein)
Nombre d’équivalents temps plein prévus
2017-2018 |
Nombre d’équivalents temps plein réels
2017-2018 |
Écart (nombre d’équivalents temps plein réels moins nombre d’équivalents temps plein prévus)
2017-2018 |
| 13,0 |
11,6 |
(1,4) |
En 2017-2018, le CEPMB a poursuivi ses activités de communication dans le but de continuer à établir des partenariats stratégiques, de sensibiliser le public à son mandat de protection des consommateurs et d’élargir la portée de ses rapports afin d’attirer davantage d’intervenants. Cela comprenait des campagnes Twitter ciblées et des engagements plus conventionnels (p. ex. par courriel et par téléphone) avec les médias nationaux, internationaux et spécialisés, y compris CBC, CTV, Radio-Canada, La Presse, The Globe and Mail, le Toronto Star, le Journal de l’Association médicale canadienne, Benefits Canada, CBS, Bloomberg News et Boston Globe, entre autres.
Le CEPMB a également continué d’appuyer et de renforcer ses activités de participation au SNIUMP en consultant régulièrement le Comité consultatif du SNIUMP, en participant à des conférences et à des comités d’intervenants, en organisant des séances d’échange d’information avec les chercheurs et en organisant des séances d’information avec les intervenants intéressés afin de partager les résultats des études analytiques. En 2017-2018, le CEPMB a publié deux rapports analytiques et sept affiches. La première étude, Concordance des listes de médicaments des régimes publics au Canada – Partie 1 : Aperçu généralNotes de bas de page vi, ainsi que la Liste des médicaments sélectionnés pour analyseNotes de bas de page vii, ont été publiées en octobre 2017 et sont disponibles sur la page des études analytiques du site Web du CEPMB. Cette étude est le premier rapport d’une série de trois rapports faisant l’analyse des lacunes et des chevauchements entre les listes publiques provinciales, territoriales et fédérales de médicaments. En février 2018, le CEPMB a publié Génériques360 – Médicaments génériques au Canada, 2016Notes de bas de page viii. Ce rapport met à jour les recherches antérieures du CEPMB (CEPMB 2014) et met l’accent sur les tendances récentes des prix des médicaments génériques au Canada, les comparaisons des prix internationaux et les analyses des segments de marché.
De plus, le CEPMB a publié son Rapport annuel 2016Notes de bas de page ix et le Document d'orientation sur les lignes directrices du CEPMBNotes de bas de page x.
Ce programme ne comporte aucun programme de niveau inférieur.
Services internes
Description
On entend par services internes les groupes d’activités et de ressources connexes que le gouvernement fédéral considère comme des services de soutien aux programmes ou qui sont requis pour respecter les obligations d’une organisation. Les services internes renvoient aux activités et aux ressources de 10 catégories de services distinctes qui soutiennent l’exécution des programmes au sein de l’organisation, sans égard au modèle de prestation des services internes du ministère. Les 10 catégories de services sont : services de gestion et de surveillance, services des communications, services juridiques, services de gestion des ressources humaines, services de gestion des finances, services de gestion de l’information, services des technologies de l’information, services de gestion des biens, services de gestion du matériel et services de gestion des acquisitions.
Résultats
Ressources financières budgétaires (en dollars)
Budget principal des dépenses
2017-2018 |
Dépenses prévues
2017-2018 |
Autorisations totales pouvant être utilisées
2017-2018 |
Dépenses réelles (autorisations utilisées)
2017-2018 |
Écart (dépenses réelles moins dépenses prévues)
2017-2018 |
| 2 584 153 |
2 584 153 |
2 699 199 |
2 629 270 |
45 117 |
Ressources humaines (équivalents temps plein)
Nombre d’équivalents temps plein prévus
2017-2018 |
Nombre d’équivalents temps plein réels
2017-2018 |
Écart (nombre d’équivalents temps plein réels moins nombre d’équivalents temps plein prévus)
2017-2018 |
| 20,0 |
18,0 |
(2,0) |
En 2017-2018, le CEPMB a retenu les services de Services publics et d’Approvisionnement Canada (SPAC) pour numériser les collections du CEPMB. À la fin de l’exercice, le SPAC avait fourni une version préliminaire de document sur les exigences opérationnelles afin de faciliter les services de numérisation. Le CEPMB a également entrepris des efforts de nettoyage physique afin de se départir des documents non requis et de trouver d’autres documents à numériser.
Le CEPMB a également amélioré son système de gestion des documents électroniques (SGDI) afin d’offrir aux utilisateurs une plus grande souplesse pour le téléchargement de documents, ainsi qu’une fonctionnalité améliorée de production de rapports et d’extraction de données. De plus, des modifications ont été apportées pour améliorer la stabilité de l’application et simplifier le modèle-type de contenu pour tenir compte de la saisie des métadonnées dans SharePoint. Les travaux d’amélioration du SGDI se poursuivront en 2018-2019.
Enfin, le CEPMB a continué de renforcer ses processus opérationnels en vue d’accroître leur valeur pour l’organisation et de réduire le fardeau administratif. Plus particulièrement, le CEPMB a numérisé tous ses processus de dotation et éliminé les justifications et les exigences de signature en double, réduisant ainsi le fardeau administratif de ses gestionnaires. La tenue de réunions régulières avec les gestionnaires pour répondre de façon proactive à leurs besoins a renforcé la planification des ressources humaines (RH), la rendant plus précieuse pour l’organisation.
Analyse des tendances en matière de dépenses et de ressources humaines
Dépenses réelles
Graphique des tendances relatives aux dépenses du Ministère
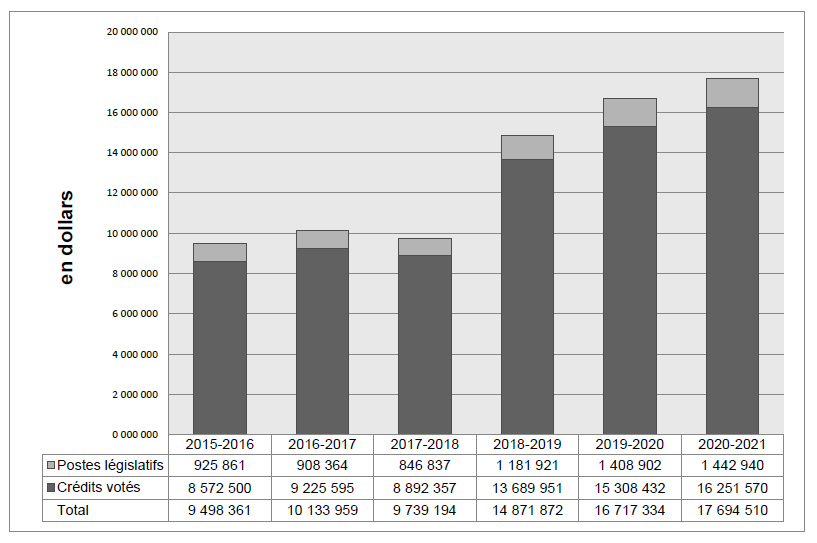
Graphique des tendances relatives aux dépenses du Ministère
Le graphique à barres ci-après illustre les tendances des dépenses du CEPMB au fil du temps. Il présente les dépenses législatives et les dépenses votées réelles pour les exercices 2015-2016 à 2017-2018, ainsi que les dépenses législatives et les dépenses votées prévues pour les exercices 2018-2019 et 2020-2021.
blank
| |
2015-2016 |
2016-2017 |
2017-2018 |
2018-2019 |
2019-2020 |
2020-2021 |
| Postes législatif |
925 861 |
908 364 |
846 837 |
1 181 921 |
1 408 902 |
1 442 940 |
| Crédits votés |
8 572 500 |
9 225 595 |
8 892 357 |
13 689 951 |
15 308 432 |
16 251 570 |
| Total |
9 498 361 |
10 133 959 |
9 739 194 |
14 871 872 |
16 717 334 |
17 694 510 |
Les dépenses votées en 2017-2018 ont été inférieures aux dépenses votées en 2016-2017 en raison, en grande partie, de la diminution des dépenses pour les audiences, contrebalancée par des paiements rétroactifs aux employés dans le cadre des négociations collectives. En 2017-2018, le CEPMB a dépensé 893 209 $ du crédit « affectation à but spécial » (ABS), comparativement à 1 883 121 $ en 2016-2017, soit une différence de 989 912 $.
Comme il a été annoncé dans le budget de 2017, le CEPMB a reçu des fonds supplémentaires pour les années à venir; 3 849 215 $ en 2018-2019, 5 694 677 $ en 2019-2020, 6 671 853 $ en 2020-2021, 7 668 725 $ en 2021-2022 et 5 680 633 $ en 2022-2023, y compris le RASE et un financement accru pour l’ABS.
Les prévisions des dépenses de 2018-2019 et des années ultérieures sont fondées sur l’hypothèse que la totalité des fonds de l’ABS destinée à la tenue d’audiences publiques sera dépensée. On procède de cette façon, car ces dépenses dépendront du nombre d’audiences, mais aussi de leur longueur et de leur complexité, qui sont difficiles à prévoir.
Sommaire du rendement budgétaire pour les programmes et les services internes (en dollars)
| Programmes et services internes |
Budget principal des dépenses
2017-2018 |
Dépenses prévues
2017-2018 |
Dépenses prévues
2018-2019 |
Dépenses prévues
2019-2020 |
Autorisations totales pouvant être utilisées
2017-2018 |
Dépenses réelles (autorisations utilisées)
2017-2018 |
Dépenses réelles (autorisations utilisées)
2016-2017 |
Dépenses réelles (autorisations utilisées)
2015-2016 |
| Programme de réglementation du prix des médicaments brevetés |
6 706 989 |
a6 706 989 |
9 298 755 |
11 358 172 |
7 189 268 |
5 611 178 |
b6 098 659 |
5 399 127 |
| Programme sur les tendances relatives aux produits pharmaceutiques |
1 575 179 |
1 575 179 |
1 928 251 |
2 087 393 |
1 547 082 |
1 498 746 |
1 616 278 |
1 688 584 |
| Total partiel |
8 282 168 |
8 282 168 |
11 227 006 |
13 445 565 |
8 736 350 |
7 109 924 |
7 714 937 |
7 087 711 |
| Services internes |
2 584 153 |
2 584 153 |
3 644 866 |
3 271 769 |
2 699 199 |
2 629 270 |
2 419 022 |
2 410 650 |
| Total |
10 866 321 |
10 866 321 |
c14 871 872 |
16 717 334 |
11 435 549 |
9 739 194 |
10 133 959 |
9 498 361 |
a Les dépenses réelles en 2017-2018 ont été inférieures aux dépenses réelles en 2016-2017 en raison, en grande partie, de la diminution des dépenses pour les audiences, contrebalancée par des paiements rétroactifs aux employés dans le cadre des négociations collectives. En 2017-2018, le CEPMB a dépensé 893 209 $ de l’ABS, comparativement à 1 883 121 $ en 2016-2017, soit une différence de 989 912 $.
b Tel qu’annoncé dans le budget de 2017, le CEPMB a reçu des fonds supplémentaires pour les années à venir : 3 849 215 $ en 2018-2019, 5 694 677 $ en 2019-2020, 6 671 853 $ en 2020-2021, 7 668 725 $ en 2021-2022 et 5 680 633 $ en 2022-2023 et de façon continue pour les exercices subséquents, incluant les paiements d’avantages sociaux des employés (PAE) et l’augmentation du crédit ABS.
c Les prévisions des dépenses de 2018-2019 et des années ultérieures sont fondées sur l’hypothèse que la totalité des fonds de l’ABS destinée à la tenue d’audiences publiques sera dépensée. On procède de cette façon, car ces dépenses dépendront du nombre d’audiences, mais aussi de leur longueur et de leur complexité, qui sont difficiles à prévoir.
Ressources humaines réelles
Sommaire des ressources humaines pour les programmes et les services internes
(équivalents temps plein)
| Programmes et services internes |
Équivalents temps plein réels
2015-2016 |
Équivalents temps plein réels
2016-2017 |
Équivalents temps plein prévus
2017-2018 |
Équivalents temps plein réels
2017-2018 |
Équivalents temps plein prévus
2018-2019 |
Équivalents temps plein prévus
2019-2020 |
| Programme de réglementation du prix des médicaments brevetés |
31,1 |
31,1 |
33,0 |
30,7 |
38,3 |
46,8 |
| Programme sur les tendances relatives aux produits pharmaceutiques |
9,2 |
13,3 |
13,0 |
11,6 |
12,7 |
13,7 |
| Total partiel |
33,9 |
44,4 |
46,0 |
42,3 |
51,0 |
60,5 |
| Services internes |
22,3 |
19,3 |
20,0 |
18,0 |
21,0 |
21,5 |
| Total |
56,2 |
63,7 |
66,0 |
60,3 |
a72,0 |
82,0 |
a Tel qu’il a été annoncé dans le Budget de 2017, le CEPMB a reçu des fonds additionnels pour les années à venir; certains de ces fonds seront utilisés pour doter d’autres postes d’ETP.
Dépenses par crédit voté
Pour obtenir des renseignements sur les dépenses votées et les dépenses législatives du CEPMB, consulter les Comptes publics du Canada de 2017-2018Notes de bas de page xi.
Dépenses et activités du gouvernement du Canada
Des renseignements sur l’harmonisation des dépenses du CEPMB avec les activités et dépenses du gouvernement du Canada sont accessibles dans l’InfoBase du GCNotes de bas de page xii.
États financiers et faits saillants des états financiers
États financiers
Les états financiers (non audités) du CEPMB pour l’exercice se terminant le 31 mars 2018 se trouvent sur le site Web du MinistèreNotes de bas de page xiii.
Faits saillants des états financiers
État condensé des opérations (non audité) pour l’exercice se terminant le 31 mars 2018 (en dollars)
| Renseignements financiers |
Résultats prévus
2017-2018 |
Résultats réels
2017-2018 |
Résultats réels
2016-2017 |
Écart (résultats réels 2017-2018 moins résultats prévus 2017-2018) |
Écart (résultats réels 2017-2018 moins résultats réels 2016-2017) |
| Total des charges |
11 991 436 |
11 175 045 |
11 140 340 |
(816 391) |
34 705 |
| Total des revenus |
- |
686 |
9 297 |
686 |
(8 611) |
| Coût de fonctionnement net avant le financement du gouvernement et les transferts |
11 991 436 |
11 174 359 |
11 131 043 |
(817 077) |
43 316 |
État condensé de la situation financière (non audité) au 31 mars 2018 (en dollars)
| Renseignements financiers |
2017–18 |
2016–17 |
Écart
(2017-2018 moins
2016-2017) |
| Total des passifs nets |
2 087 459 |
2 294 983 |
(207 524) |
| Total des actifs financiers nets |
1 307 889 |
1 722 674 |
(414 785) |
| Dette nette du Ministère |
779 570 |
572 309 |
207 261 |
| Total des actifs non financiers |
120 272 |
100 895 |
19 377 |
| Situation financière nette du Ministère |
(659 298) |
(471 414) |
(187 884) |
Renseignements supplémentaires
Renseignements ministériels
Profil organisationnel
Ministre de tutelle : L’honorable Ginette Petitpas Taylor
Administrateur général : Dr Mitchell Levine, Président
Portefeuille ministériel : Santé
Instrument habilitant : Loi sur les brevetsNotes de bas de page xiv et Règlement sur les médicaments brevetésNotes de bas de page xv
Année d’incorporation ou de création : 1987
Autres : Le ministre de la Santé est responsable de l’application des dispositions de la Loi sur les brevets (la Loi) formulées aux articles 79 à 103. Même s’il fait partie du portefeuille de la Santé, le Conseil d’examen du prix des médicaments brevetés, en raison de ses responsabilités quasi judiciaires, exerce son mandat en toute indépendance vis-à-vis du ministre de la Santé. Il fonctionne également d’une façon indépendante de Santé Canada, qui autorise la vente des médicaments au Canada après avoir vérifié leur innocuité, leur efficacité et leur qualité, d’autres membres du portefeuille de la santé, comme l’Agence de la santé publique du Canada, les Instituts de recherche en santé du Canada et l’Agence canadienne d’inspection des aliments, les régimes publics fédéral, provinciaux et territoriaux d’assurance-médicaments qui autorisent l’inscription des médicaments sur leurs formulaires de médicaments admissibles à un remboursement et le Programme commun d’examen des médicaments, géré par l’Association canadienne des médicaments et des technologies de la santé (ACMTS), qui évalue l’efficience des médicaments avant leur inscription sur les formulaires des régimes publics d’assurance-médicaments participants.
Cadre de présentation de rapports
Le résultat stratégique et l’architecture d’alignement des programmes officiels du CEPMB pour 2017-2018 sont présentés ci-dessous.
1. Résultat stratégique : Les médicaments brevetés ne peuvent être vendus au Canada à des prix excessifs, afin de protéger les intérêts de la population canadienne. La population canadienne est également tenue informée sur les tendances concernant les produits pharmaceutiques.
1.1 Programme : Programme de réglementation du prix des médicaments brevetés
1.2 Programme : Programme sur les tendances relatives aux produits pharmaceutiques
Services internes
Renseignements connexes sur les programmes de niveau inférieur
Le CEPMB ne compte pas de programmes de niveau inférieur. Il n’a qu’un seul objectif stratégique, deux programmes de soutien et des services internes.
Tableaux de renseignements supplémentaires
Les tableaux de renseignements supplémentaires qui suivent sont accessibles sur le site Web du CEPMB :
Dépenses fiscales fédérales
Il est possible de recourir au régime fiscal pour atteindre des objectifs de la politique publique en appliquant des mesures spéciales, comme de faibles taux d’impôt, des exemptions, des déductions, des reports et des crédits. Le ministère des Finances Canada publie chaque année des estimations et des projections du coût de ces mesures dans le Rapport sur les dépenses fiscales fédéralesNotes de bas de page xvii. Ce rapport donne aussi des renseignements généraux détaillés sur les dépenses fiscales, y compris les descriptions, les objectifs, les renseignements historiques et les renvois aux programmes des dépenses fédéraux connexes. Les mesures fiscales présentées dans ce rapport relèvent du ministre des Finances.
Coordonnées de l’organisation
Conseil d’examen du prix des médicaments brevetés
C.P. L40
Centre Standard Life
333, avenue Laurier Ouest
Bureau 1400
Ottawa (Ontario) K1P 1C1
Téléphone : (613) 288-9635
Sans frais : 1-877-861-2350
Télécopieur : (613) 288-9643
AST : (613) 288-9654
Courriel : PMPRB.Information-Renseignements.CEPMB@pmprb-cepmb.gc.ca
Site Web : www.pmprb-cepmb.gc.ca
Annexe : définitions
analyse comparative entre les sexes plus (ACS+) (gender-based analysis plus [GBA+])
Approche analytique qui sert à évaluer les répercussions potentielles des politiques, des programmes ou des initiatives sur divers ensembles de personnes (femmes, hommes ou autres). L’identité individuelle est déterminée par une multitude de facteurs en plus du sexe, par exemple la race, l’origine ethnique, la religion, l’âge ou le fait de vivre avec un handicap de nature physique ou intellectuelle. D’où l’ajout du mot « plus », signifiant que l’analyse ne se limite pas au sexe (différences biologiques) ou au genre (la construction sociale du sexe), mais considère aussi les autres facteurs qui les recoupent. Un processus d’ACS+ pourrait être, à titre d’exemple, le recours à des données ventilées selon le sexe, le genre et d’autres facteurs identitaires pour les analyses du rendement, et la détermination de toute répercussion du programme sur divers groupes de personnes dans l’optique de modifier les initiatives pour les rendre plus inclusives.
architecture d’alignement des programmes (Program Alignment Architecture)
Répertoire structuré de tous les programmes d’un ministère ou organisme qui décrit les liens hiérarchiques entre les programmes et les liens aux résultats stratégiques auxquels ils contribuent.
cible (target)
Niveau mesurable du rendement ou du succès qu’une organisation, un programme ou une initiative prévoit atteindre dans un délai précis. Une cible peut être quantitative ou qualitative.
crédit (appropriation)
Autorisation donnée par le Parlement d’effectuer des paiements sur le Trésor.
dépenses budgétaires (budgetary expenditures)
Dépenses de fonctionnement et en capital; paiements de transfert à d’autres ordres de gouvernement, à des organisations ou à des particuliers; et paiements à des sociétés d’État.
dépenses législatives (statutory expenditures)
Dépenses approuvées par le Parlement à la suite de l’adoption d’une loi autre qu’une loi de crédits. La loi précise les fins auxquelles peuvent servir les dépenses et les conditions dans lesquelles elles peuvent être effectuées.
dépenses non budgétaires (non budgetary expenditures)
Recettes et décaissements nets au titre de prêts, de placements et d’avances, qui modifient la composition des actifs financiers du gouvernement du Canada.
dépenses prévues (planned spending)
En ce qui a trait aux plans ministériels et aux rapports sur les résultats ministériels, les dépenses prévues s’entendent des montants approuvés par le Conseil du Trésor au plus tard le 1er février. Elles peuvent donc comprendre des montants qui s’ajoutent aux dépenses prévues indiquées dans le budget principal des dépenses.
Un ministère est censé être au courant des autorisations qu’il a demandées et obtenues. La détermination des dépenses prévues relève du ministère, et ce dernier doit être en mesure de justifier les dépenses et les augmentations présentées dans son plan ministériel et son rapport sur les résultats ministériels.
dépenses votées (voted expenditures)
Dépenses approuvées annuellement par le Parlement par une loi de crédits. Le libellé de chaque crédit énonce les conditions selon lesquelles les dépenses peuvent être effectuées.
équivalent temps plein (full time equivalent)
Mesure utilisée pour représenter une année-personne complète d’un employé dans le budget ministériel. Les équivalents temps plein sont calculés par un rapport entre les heures de travail assignées et les heures de travail prévues. Les heures normales sont établies dans les conventions collectives.
évaluation (evaluation)
Au sein du gouvernement du Canada, collecte et analyse systématiques et neutres de données probantes en vue d’évaluer le bien-fondé, le mérite ou la valeur. L’évaluation guide la prise de décisions, les améliorations, l’innovation et la reddition de comptes. Elle porte habituellement sur les programmes, les politiques et les priorités et examine des questions se rapportant à la pertinence, à l’efficacité et à l’efficience. Toutefois, selon les besoins de l’utilisateur, l’évaluation peut aussi examiner d’autres unités, thèmes et enjeux, notamment des solutions de rechange aux interventions existantes. L’évaluation utilise généralement des méthodes de recherche des sciences sociales.
expérimentation (experimentation)
Activités visant à étudier, mettre à l’essai et comparer les effets et les répercussions de politiques, d’interventions et d’approches pour savoir ce qui fonctionne et ne fonctionne pas, et à étayer la prise de décision sur des éléments probants.
indicateur de rendement (performance indicator)
Moyen qualitatif ou quantitatif de mesurer un extrant ou un résultat en vue de déterminer le rendement d’une organisation, d’un programme, d’une politique ou d’une initiative par rapport aux résultats attendus.
initiative horizontale (horizontal initiative)
Initiative dans le cadre de laquelle deux organisations fédérales ou plus reçoivent du financement dans le but d’atteindre un résultat commun, souvent associé à une priorité du gouvernement.
plan (plan)
Exposé des choix stratégiques qui montre comment une organisation entend réaliser ses priorités et obtenir les résultats connexes. De façon générale, un plan explique la logique qui sous-tend les stratégies retenues et tend à mettre l’accent sur des mesures qui se traduisent par des résultats attendus.
plan ministériel (Departmental Plan)
Exposé des plans et du rendement attendu d’un ministère qui reçoit des crédits parlementaires. Les plans ministériels couvrent une période de trois ans et sont présentés au Parlement au printemps.
priorité (priority)
Plan ou projet qu’une organisation a choisi de cibler et dont elle rendra compte au cours de la période de planification. Il s’agit de ce qui importe le plus ou qui doit être fait en premier pour appuyer la réalisation du ou des résultats stratégiques souhaités.
priorités pangouvernementales (government-wide priorities)
Aux fins du Rapport sur les résultats ministériels 2017-2018, les thèmes de haut niveau qui présentent le programme du gouvernement issu du discours du Trône de 2015 (c’est-à-dire la croissance de la classe moyenne, un gouvernement ouvert et transparent, un environnement sain et une économie forte, la diversité en tant que force du Canada, ainsi que la sécurité et les possibilités).
production de rapports sur le rendement (performance reporting)
Processus de communication d’information sur le rendement fondée sur des éléments probants. La production de rapports sur le rendement appuie la prise de décisions, la responsabilisation et la transparence.
programme (program) (s’applique aux ministères dont le rapport est fondé sur l’architecture d’alignement des programmes)
Groupe de ressources et d’activités connexes géré de manière à répondre à des besoins précis et à atteindre les résultats visés; ces ressources et activités sont traitées comme une unité budgétaire.
programme temporisé (sunset program)
Programme ayant une durée fixe et dont le financement et l’autorisation politique ne sont pas permanents. Lorsqu’un tel programme arrive à échéance, une décision doit être prise quant à son maintien. Dans le cas d’un renouvellement, la décision précise la portée, le niveau de financement et la durée.
rapport sur les résultats ministériels (Departmental Results Report)
Rapport d’un ministère recevant des crédits parlementaires qui présente les réalisations réelles par rapport aux plans, aux priorités et aux résultats attendus énoncés dans le plan ministériel correspondant.
rendement (performance)
Utilisation qu’une organisation a faite de ses ressources en vue d’obtenir ses résultats, mesure dans laquelle ces résultats se comparent à ceux que l’organisation souhaitait obtenir, et mesure dans laquelle les leçons apprises ont été cernées.
résultat (result)
Conséquence externe attribuable en partie aux activités d’une organisation, d’une politique, d’un programme ou d’une initiative. Les résultats ne relèvent pas d’une organisation, d’une politique, d’un programme ou d’une initiative unique, mais ils s’inscrivent dans la sphère d’influence de l’organisation.
résultat stratégique (Strategic Outcome)
Avantage durable et à long terme pour les Canadiens qui est rattaché au mandat, à la vision et aux fonctions de base d’une organisation.
structure de gestion, des ressources et des résultats (Management, Resources and Results Structure)
Cadre global qui consiste en un répertoire des programmes, des ressources, des résultats, des indicateurs de rendement et de l’information sur la gouvernance d’une organisation. Les programmes et les résultats sont décrits en fonction du lien hiérarchique qui les unit, ainsi que du ou des résultats stratégiques auxquels ils contribuent. La structure de gestion, des ressources et des résultats est élaborée à partir de l’architecture d’alignement des programmes.